La Tabla Periódica PDF

| Title | La Tabla Periódica |
|---|---|
| Author | Aracely Chiluisa |
| Course | Química |
| Institution | Universidad Rey Juan Carlos |
| Pages | 29 |
| File Size | 1.7 MB |
| File Type | |
| Total Downloads | 105 |
| Total Views | 128 |
Summary
Tema sobre la tabla periodica...
Description
1. La Tabla Peridica La tabla Peridica es una tabla en la que se encuentran agrupados los elementos que tienen propiedades quimicas y fisicas semejantes. Los elementos est n acomodados de acuerdo con su nmero atmico en: ❑Filas horizontales, llamadas periodos ❑ Columnas verticales, conocidas como grupos o familias ❑ Los elementos de los grupos 3 a 11 se denominan Elementos de transicin. ❑ Otra manera de poder nombrar los diferentes grupos de la Tabla Peridica es con el nombre del primer elemento de cada grupo. Por ej. el grupo del boro sera: el grupo B, Al, Ga, In y Tl. • • • • •
Metales Alcalinos: Li, Na, K , Rb, Cs y Fr Metales Alcalinotrreos: Be, Mg, Ca, Sr, Ba, y Ra. Calcgenos: O, S, Se, Te, Po. Halgenos: F, Cl, Br I, At. Gases Nobles: He, Ne, Ar , Kr, Xe Rn.
Electronegatividad: medida del poder de un tomo o de un grupo para atraer electrones. ❑Es uno de los criterios utilizados para establecer la prioridad o la precedencia de un elemento respecto a otro. ❑ Se deben escribir segn las EN relativas, es decir, se coloca primero el elemento menos electronegativo y despues el mas electronegativo 2.
3. Nmero de oxidacin El nmero o estado de oxidacin de un tomo en una entidad molecular es un nmero positivo, negativo o cero, que representa la carga que quedar a en el tomo dado, si los pares electrnicos de cada enlace que forma se asignan al miembro ms electronegativo del par de enlace. Convencionalmente se supone que 1. El nºde oxidacin de un in simple = su carga. 2. En un elemento, su nºde oxidacin es cero. 3. La suma de los unº de oxidacin de los tomos que constituyen un compuesto, multiplicados por los correspondientes subndices, es cero si el compuesto es neutro, o igual a su carga neta en el caso de ser un anin o un cati n. 4. El nmero de oxidacin del hidrgeno es I cuando se combina con elementos no metlicos y –I cuando se combina con elementos met licos. 5. El nmero de oxidacin del oxgeno – II, salvo en perxidos que es – I. 6. Los grupos orgnicos unidos a tomos metlicos se tratan unas veces como aniones (por ejemplo, el ligando metilo se considera habitualmente que es el ion metanuro –CH3) y otras veces como neutros (por ej, el mon xido de carbono, CO). 7. Los enlaces entre tomos de la misma especie no contribuyen al nmero de oxidacin. Se puede indicar el estado de oxidacin de un elemento en una frmula y para ello se debe escribir como superindice a la derecha del elemento y en numeros romanos. El estado de oxidacion cero se representa con 0 aunque generalmente no se escribe. Ejemplo: K[OsVIII (N)O3 ] Nmero de oxidacin Es posible que se trate de un compuesto con un mismo tomo en dos estado de oxidacin distintos, lo que da un estado de oxidacin extrao para el elemento, en este caso, el s mbolo del elemento se debe repetir y cada smbolo se le asigna un nmero de oxidacin en una secuencia creciente. Ejemplo: Ejemplo:
O -2 PbIIPbIVO = Pb O 2434 Tambin cuando no es razonable definir el estado de oxidacin de un elemento dentro del grupo (ej. Hiperoxido) se recomienda expresar el estado de oxidacion total del grupo por medio de una carga ionica formal, evitando de esta manera el uso de estados de oxidacin fraccionados. Nmero de oxidacin ms usuales Los elementos de los grupos principales y los del grupo 12, presentan los siguientes estados de oxidacin como ms usuales Grupo 1 Grupo 2 Grupo 13 Grupo 14 Grupo 15 Grupo16 Grupo 17 Grupo 12 Li, Na, K, Rb, Cs, Fr +I Be, Mg, Ca, Ba, Sr, Ra +II B +III /// -III, Al +III, Ga +III, In +III, +I; Tl +III, +I. C +IV /// -IV; Si +IV///-IV; Ge +IV,+II; Sn +IV,+II, Pb +IV, +II N +V,+IV,+III,+II,+I /// -III; P +V,+III,+I /// -III; As +V,+III /// -III; Sb +V,+III /// -III;,Bi +V, +III. O –II; S +IV,+VI, +II /// -II; ,Se +IV,+VI, +II /// -II,Te +IV,+VI, +II /// -II, Po +IV, +II. F –I, Cl +VII, +V, +III, +I /// -I,Br +VII, +V, +III, +I /// -I,I +VII, +V, +III, +I /// -I, At +VII, +V, +III, +I /// -I. Zn +II, Cd +II, Hg +II, +I 6 Para los elementos de transicin presentan una gran variedad de estados de oxidacin. Grupo 3 Grupo 4 Grupo 5 Grupo 6 Grupo 7 Grupo 8 Grupo 9 Grupo 10 Grupo 11 Sc +III, Y+III, La +III, Ac +III Ti +II, +III, +IV, Zr +II, +III, +IV, Hf +III, +IV V +II, +III, +IV, +V, Nb +III, +IV, +V, Ta +III, +IV, +V Cr +II, +III, +IV, +V, +VI, Mo +II, +III, +IV, +V, +VI,, W +II, +III, +IV, +V, +VI. Mn +II, +III, +IV, +V, +VI, +VII,Tc +IV, +V, +VI, VII, Re +IV, +V, +VI, VII. Fe +II, +III; Ru +II a +VII, Os +II a +VII Co +II, +III , Rh +III +IV, +VI, Ir +III, +IV, +VI Ni +II, +III., Pd +II, +IV, Pt +II, +IV, +VI Cu +I, +II, Ag +I, Au +I, +III Nmero de oxidacin ms usuales Finalmente los estados de oxidacin elementos de transici n interna son: Lantanoides Ce +III, +IV Pr +III, +IV Nd +III, +IV, +II Pm +III Sm +III, +II Eu +III,+II Gd +III Tb +III, +IV Dy +III, +IV Ho +III Er +III Tm +III, +II Yb +III,+II Lu +III ms habituales de los Actinoides Th +III, +IV Pa +III, +IV, +V
U +III, +IV, +V, +VI Np +III, +IV, +V, +VI Pu +III, +IV, +V, +VI Am +III,+IV,+V,+VI Cm +III, +IV Bk +III, +IV Cf +III Es +III Fm +III Md +III No ¿? Lr ¿? 14.4. Nombres de los elementos El nombre de los primeros elementos descubiertos fue dado en relacin a su origen, propiedades fsicas o qumicas, etc, y ms recientemente en conmemoracin de eminentes cientficos. Desde 1947 los descubridores sugieren el nombre del elemento descubierto a la Divisin Qumica Inorgnica quin har la recomendacin a la IUPAC que tomar la decisin final. Mientras que los nuevos elementos no tienen un nombre aprobado, se puede referir a ellos mediante un nombre sistematico y un simbolo de 3 letras. Este nombre deriva directamente de su nmero atmico utilizando las siguientes races: 0= nil 3= tri 6= hex 9= enn 1= un 4= quad 7= sept 2= bi 5= pent 8=oct Nombres de los elementos Las reglas para nombrar a un compuesto son: ❑ Se deben colocar estas races juntas en el orden de los dgitos del nmero atmico. ❑ A continuaci n se aade el sufijo “io”. ❑ Cuando “bi” o “tri” es el nmero antes del sufijo se elimina la i final, as como tambin se elimina la n de “enn” cuando est colocado delante de 0 (nil). ❑ El smbolo del elemento sera la primera letra de cada una de estas races. No atmico Smbolo 113 Uut 120 Ubn 200 Bnn 400 Qnn Nombre ununtrio unbinilio binilnilio cuadnilnilio Andrs Garcs Osado 8 Grado de Biologa 08/10/2015 Nombres de los elementos Los ltimos elementos nombrados han sido el 114 y 116 que se han llamado Flevorio (Fl), y Livermorio (Lv). Los elementos ms recientemente descubiertos han sido ❑Rutherfordio, Rf Grupo 4, elemento 104 ❑Dubnio, Db Grupo 5, elemento 105 ❑Seaborgio, Sg Grupo 6, elemento 106 ❑Bohrio, Bh Grupo 7, elemento 107 ❑Hassio, Hs Grupo 8, elemento 108 ❑Meitnerio, Mt Grupo 9, elemento 109 ❑Darmstadtio, Ds Grupo 10, elemento 110 ❑Roentgenio, Rg Grupo 11, elemento 111 ❑Copernicio, Cn Grupo 11, elemento 111 Smbolos de los elementos El smbolo atmico de un elemento, que consta de una, dos o tres letras se usa para representar al tomo en una frmula qumica. ste puede acompaarse de informacin complementaria, tal como se muestra: nmero msico Xcarga inica nmero atmico nmero de tomos
Cuando se indica la carga en un tomo el signo + o – se debe colocar despus del valor numrico y nunca antes, es decir: CORRECTO An+ An− INCORRECTO A+n A−n Andrs Garcs Osado 9 Grado de Biologa 08/10/2015 Istopos de los elementos Los istopos de un tomo se distinguen aadiendo el nmero msico al nombre: 18O oxgeno -18 Los is topos del hidrgeno son los nicos que poseen un nombre especial: protio (hidrgeno-1), deuterio (hidrgeno-2) y tritio (hidr geno- 3). Los smbolos para deuterio y tritio son D y T respectivamente, aunque sin embargo es preferible utilizar la misma nomenclatura que se usa para otros is topos, es decir el smbolo del elemento,en este caso H, y el no masico en el vertice superior izquierdo del mismo, es decir 2H y 3H serian los simbolos para deuterio y tritio Los cationes de los is topos de hidrgeno, 1H+ , 2H+ y 3H+ se denominan, protn, deutern y tritn. Nombres de los elementos Las sustancias que tienen una f rmula molecular indefinida o infinita, o son un mezcla de altropos , se denominan como el elemento Ejemplo: Ejemplos: Znx Zn Ambos se nombran como cinc Sin embargo aquellas formas alotrpicas de los elementos que presentan una forma molecular definida, se nombrarian anadiendo el correspondiente prefijo numeral (mono, di, tri, tetra, penta, etc) al nombre del elemento. H monohidrgeno O3 trioxgeno N mononitrgeno N 2 dinitrgeno S8 octaazufre P4 tetrafsforo Andrs Garcs Osado 10 Grado de Biologa 08/10/2015 Nombres de los elementos Si el nmero de de tomos es muy grande y desconocido se usa el prefijo “poli” Ejemplo: Ejemplos: Sn poliazufre Algunas de estas sustancias son conocidas por su nombre com n cuyo uso es permitido: O2 O3 Ozono P4 Fsforo blanco Oxgeno 14.5. Tipos de frmulas
•Frmula emprica : Esta formada por la yuxtaposici n de los smbolos atmicos con los apropiados subndices para dar la expresin de la composicin estequiomtrica del compuesto en cuestion. El orden de citacion de los s imbolos es siempre que no haya cualquier otro criterio, el orden alfabtico excepto para compuestos que contengan grupos orgnicos, donde C e H se citan primero y segundo respectivamente. Ejemplos: BrClH3N2NaO2Pt C10 H10 ClFe • Frmula molecular. La frmula molecular de un compuesto formado por molculas discretas es aquella que concuerda con la masa molecular relativa. El orden de citacin de los smbolos es distinto a la frmula emprica, como veremos ms adelante. Andrs Garcs Osado 11 Grado de Biologa 08/10/2015 Tipos de Frmulas •En algunos casos la frmula emprica se corresponde con la composicin de una sustancia y por lo tanto solo se diferenciara de la molecular en el orden de escritura de los elementos. Cuando no es posible establecer la composici n de una sustancia, por ejemplo un polmero se escribe como subndice la letra n. Ejemplos: Frmula Frmula molecular emprica S8 S Sn S8 SF FS 66 S2Cl2 SCl N2O4 NO2 Tipos de Frmulas • Frmula estructural. La frmula estructural da una completa informacin de c mo los tomos se encuentran organizados y conectados en una molcula. A veces un simple frmula da informacin de cmo se encuentran ordenados:
Andrs Garcs Osado 12 Grado de Biologa 08/10/2015 14.6. Tipos de nomenclaturas Los sistemas de nomenclatura principales en qumica inorgnica son: ❑Nomenclatura de composicin, binaria o estequiom trica. basada nicamente en la composicin de una sustancia dada y no en su estructura, siendo la nica opci n posible si no se dispone de informacin estructural ❑Nomenclatura de sustitucin o sustitutiva Es el tipo de Nomenclatura que se ha venido usando en Qumica Orgnica y donde la construccin de los nombres se hace en base a los de una serie de hidruros progenitores,
❑ Nomenclatura de Adicin o aditiva Es el tipo de Nomenclatura que se ha venido usando en Qumica de compuestos de coordinacin y donde se trata a un compuesto como la combinaci n de un tomo central o varios tomos centrales y unos grupos asociados conocidos como ligandos 14.7. Nomenclatura y formulaci n inorgnica. Cationes Monoat micos 1. K+ 2. La3+ 3. Au+ 4. Cu2+ 5. Mg2+ 6. H+ 7. 1H+ 8. 2H+ 9. 3H+ potasio(1+) lantano(3+) oro(1+) cobre(2+) magnesio(2+) hidrgeno(1+), hidrn protio(1+), protn deuterio(1+), deuteron tritio(1+), triton El nombre de estos cationes es el mismo que el del tomo aadiendo a continuacin despus del nombre y sin espacio, entre parntesis la carga apropiada con el signo + Andrs Garcs Osado 13 Grado de Biologa 08/10/2015 Nombre de iones Cationes Homopoliatmicos Se nombran utilizando el nombre estequiomtrico de la especie neutra correspondiente, es decir, el nombre del elemento con el prefijo multiplicativo adecuado, a adiendo al final el nmero de carga entre parntesis y sin espacio entre el nombre y la carga 1. O2+ 2. Si2 + 3. Hg22+ 4. S82+ 5. H3+ dioxgeno(1+) disilicio(1+) dimercurio(2+) octaazufre(2+) trihidr geno(1+) Prefijos multiplicativos 1 mono 11 undeca 21 henicosa 60 hexaconta 2 di 12 dodeca 22 docosa 70 heptaconta 3 tri 13 trideca 23 tricosa 80 octaconta 4 tetra 14 tetradeca 30 triaconta 90 nonaconta 5 penta 15 pentadeca 31 hentriaconta 100 hecta 6 hexa 16 hexadeca 35 pentatriaconta 200 dicta 7 hepta 17 heptadeca 40 tetraconta 500 pentacta 8 octa 18 octadeca 48 octatetraconta 1000 kilia 9 nona 19 nonadeca 50 Pentaconta 2000 dilia 10 deca 20 icosa 52 dopentaconta Andrs Garcs Osado 14 Grado de Biologa 08/10/2015 Nombre de iones Cationes heteropoliatmicos -Este tipo de especies se nombran habitualmente utilizando la nomenclatura de sustitucin o la nomenclatura de la adicin que no se tratan en este curso. - Adems existen todava algunos nombres no sistemticos aceptados por la IUPAC. -Su nomenclatura es extensa y complicada pues depende de cmo se ha originado el catin Algunos ejemplos de cationes habituales son: Donde los ejemplos 1 y 2 se han nombrado mediante la nomenclatura de sustituci n y los ejemplos 3 y 4 por la de adicin 1. NH4+ azanio o amonio 2. H3O+ oxidanio u oxonio 3. NO+ oxidonitrgeno(1+) 4. NO2+ dioxidonitrgeno(1+) Nombre de iones Aniones Monoatmicos
❑Estos aniones se nombran o bien reemplazando la desinencia del nombre del elemento (“eso”, “ico”, “io”, “o”, “ogeno”,”ono” u “oro”) por “-uro” o anadiendo directamente la terminacion “-uro” al nombre del elemento. ❑los nmeros de carga se pueden aadir para identificar completamente al anin, o se pueden omitir stos cuando no exista ambiguedad 1. Cl− 2. C4− 3. S2− 4. N3− 5. O2− cloruro(1−) carburo(4−) sulfuro(2−) nitruro(3−) xido(2 −) Andrs Garcs Osado 15 Grado de Biologa 08/10/2015 Nombre de iones Aniones Homopoliat micos ❑Se nombran sustituyendo la terminacin del nombre del elemento por la desinencia “-uro”. ❑El nombre debe ir precedido por un prefijo numrico, como di-, tri-, tetra-, que indique el numero de atomos presentes. ❑ Se debe acompaar siempre el nmero de carga entre parntesis al final del nombre. 1. O2- 2. O22- 3. O3- 4. C22- 5. N3dixido(1-) dixido(2-) trixido(1-) dicarburo(2-) trinitruro(1-) superxido perxido oznido acetiluro azida Nombre de iones Aniones Heteropoliat micos -Este tipo de especies se nombran habitualmente utilizando la nomenclatura de sustitucin o la nomenclatura de la adicin que no se tratan en este curso. - Adems existen todava algunos nombres no sistemticos aceptados por la IUPAC. Algunos ejemplos de aniones habituales son: 1. NH2- azanuro amida 2. NH2- azanodiuro o imida 3. HO- oxidanuro hidrxido 4. HCO3- hidrogeno(trioxidocarbonato)(1−) hidrogenocarbonato 5. CN- nitrurocarbonato(1-) cianuro 6. [ClO3]- trioxidoclorato(1-) clorato
Son las sustancias formadas por dos clases de elementos, independientemente del nmero de tomos de cada clase: NaCl, N2O4, etc... Ejemplos
Frmula: Primero se escribe el componente electropositivo seguido del componente electronegativo. El orden de electronegatividad es el de la la tabla de electronegatividad NaCl CaF FeO SiC 3234 Nombre de compuestos binarios ❑Al construir un nombre estequiomtrico de un compuesto binario, uno de los elementos se clasifica como el constituyente electropositivo y el otro como el constituyente electronegativo de acuerdo a la tabla de electronegatividad. El componente electronegativo es, por convenio, el elemento que aparece en primer lugar en la secuencia de la Tabla electronegatividad. ❑ El nombre completo se construye como sigue: Nombre del anin terminado en –uro (excepto xido) de Nombre del catin (el del elemento sin modificar)
Andrs Garcs Osado 17 Grado de Biologa 08/10/2015 Nombre de compuestos binarios ❑ Las proporciones de los constituyentes de una especie binaria se pueden indicar mediante el empleo de prefijos multiplicadores, mediante nmeros de carga o mediante numeros de oxidacion. CaBr2 bromuro de calcio (2+) MnO2 xido de manganeso (IV) N2O4 tetraxido de dinitrgeno Diferentes familias de compuestos binarios NH3 PH3 HCl CrO3 Cr2 O3 BaO2 KO2 KO3 Ca3P2 O2Cl trihidruro de nitrgeno azano amonaco trihidruro de fsforo o fosfano cloruro de hidrgeno trixido de cromo u xido de cromo(VI) trixido de dicromo u xido de cromo(III) di xido(2−) de bario perxido de bario dixido(1−) de potasio superxido de potasio trixido(1−) de potasio u oznido de potasio difosfuro de tricalcio fosfuro de calcio cloruro de dioxgeno Se trata de un tipo de combinaci n donde se puede distinguir un componente electronegativo y otro electropositivo, si bien formalmente se encuentran constituidos por 3 o mas tipos de atomos Cuando se construye el nombre utilizando prefijos multiplicadores, puede ser que un componente contenga ya un prefijo multiplicador (disulfato, difosfato, etc.). En este caso y con el fin de evitar ambiguedades, se utilizan los prefijos multiplicadores del tipo bis, tris, tetrakis, etc. Li(OH) hidr xido de litio Mg(OH)2 hidrxido de magnesio NH4Cl cloruro de amonio Ca3(PO4)2 bis(fosfato) de tricalcio Un oxo cido es un compuesto que contiene oxgeno, hidrgeno (al menos un hidrgeno debe estar unido al oxgeno) y otro elemento. ❑ Son compuestos que responden a la frmula general HaXbHcOd donde Ha son los hidrgenos cidos, y Hc son los hidruros. ❑ Los dos tipos de nomenclatura recomendados actualmente por la IUPAC para este tipo de compuestos, son la nomenclatura sistemtica de adicin y la nomenclatura vulgar o tradicional. Andrs Garcs Osado 19 Grado de Biologa 08/10/2015 Nomenclatura tradicional de oxocidos ❑Al nombre abreviado del elemento central X se le antepone la palabra cido y se le hace terminar en -oso o en -ico, segn que dicho elemento acte con el ndice de oxidacin menor a mayor respectivamente. ❑Esta regla puede extenderse en caso de que el elemento posea cuatro estados de oxidacin diferentes combinando los prefijos hipo- y per- con los sufijos -oso e -ico de la siguiente forma: Todava estn aceptados el nombre de algunos cidos que contienen los prefijos orto, meta o piro- formados por el distinto nmero de molculas de agua aadidas al xido de partida cido hipo .............oso cido cido cido per .............oso .............ico .............ico Estado de oxidacin aumenta de hacia abajo en la serie Nomenclatura tradicional de oxo cidos HClO HClO2 HClO3 HClO4 HIO3 HIO4 H3PO4 H2SO4
H2S2O7 H2CO3 H2SO3 HNO2 HNO3 cido hipocloroso cido cloroso cido clrico cido percl rico cido ydico cido perydico cido fosfrico ortofosfrico cido sulfrico cido disulfrico cido carbnico cido sulfuroso cido nitroso cido ntrico Andrs Garcs Osado 20 Grado de Biologa 08/10/2015 Nomenclatura sistemtica de oxocidos ❑Los nombres de estos compuestos, seg n la nomenclatura adicin, se construyen citando los tomos o grupos de tomos unidos al tomo central o ligandos en orden alfabtico, delante del nombre del tomo central. El tomo central se debe seleccionar el que es relativamente central en la estructura. Si existe alternativa se toma como central el que se encuentra el ltimo en la escala de electronegatividad. HClO2= [ClO(OH)] H2SO4 = [SO2(OH)2] H2TeO4 = [TeO2(OH)2] HNO2 = [NO(OH)] H2PHO3 = [PHO(OH)2] hidroxidooxidocloro dihidroxidodioxidoazufre dihidroxidodioxidoteluro hidroxidooxidonitrgeno dihidroxidohidrurooxidofsforo Son compuestos constituidos por tres tipos distintos de iones que deben entenderse como sales generalizadas. Sal generalizada es cualquier compuesto en el que se puede identificar al menos un ion positivo, o que puede clasificarse como electropositivo, o que es ms electropositivo que los dems constituyentes y, al menos, un ion negativo o que puede clasificarse como electronegativo, o que es ms electronegativo que el resto de los constituyentes. El principio de ordenacin de los iones en este tipo de compuestos se basa en que: 1. Todos los constituyentes electropositivos preceden a todos los constituyentes electronegativos. 2. Se usa el orden alfabtico dentro de cada uno de los dos grupos que constituyen la frmula. Andrs Garcs Osado 21 Grado de Biologa 08/10/2015 Especies ternarias ❑ Se nomb...
Similar Free PDFs

La Tabla ASCII-Cuadro
- 2 Pages

La Tabla Periódica
- 29 Pages

La tabla periodica
- 10 Pages

Historia DE LA Tabla Periódica
- 1 Pages

Historia de la tabla periódica
- 5 Pages

Plantilla de la Tabla Periódica
- 2 Pages

Elementos DE LA Tabla Periodica
- 5 Pages

Evolución de la Tabla Periódica
- 5 Pages
Tabla
- 5 Pages
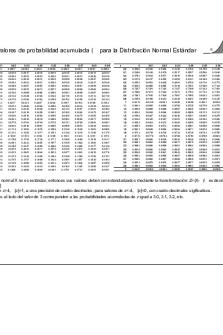
Tabla-z - Tabla Z
- 1 Pages

Tabla-z - tabla de z
- 1 Pages

Tabla para llenar la base de datos
- 160 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu



