Física quàntica simplificada PDF

| Title | Física quàntica simplificada |
|---|---|
| Course | Física II |
| Institution | Bachillerato (España) |
| Pages | 10 |
| File Size | 319.6 KB |
| File Type | |
| Total Downloads | 108 |
| Total Views | 137 |
Summary
Sintetizar la física cuántica para alumnos que justo se introducen al tema....
Description
Física cuántica
Martí Baeza Aiman Himi Nina Righelato David Oliva
Índex I.- El descobriment de la física quàntica…………………………………………..pàg 2 II.- Interpretació Quàntica de l'àtom………………………………………………..pàg 3 III.- Experiment de la doble escletxa………………………………………………..pàg 5 IV.- La funció d’ona i al regla de Born………………………………………………pàg 8 V.- El principi d’incertesa de Heisenberg………………………………………...pàg 10
1
I.
El descobriment de la física quàntica
Els primers indicis que va tenir la humanitat de l'univers quàntic van aparèixer el 1900 amb Max Planck, un físic brillant que tractava d'esbrinar perquè els objectes canviaven de color a l'escalfar-se. Max Planck ens va introduir en l'era quàntica, va traçar de desxifrar el misteri de perquè els objectes can
vien de color a l'escalfar-se, cosa que potser sembla inútil, però
gràcies a aquesta inquietud igual ara no existiria la física cuántica. Volia utilitzar aquest mètode per entendre perquè els objectes canviaven de color a l'escalfar -se, el que va descobrir va ser que les lleis de la física clàssica no funcionaven, la resposta que donaven no era valida, de manera que va intentar aplicar un mètode completament nou un conjunt d'hipòtesis matemàtiques noves i va funcionar, va aconseguir la resposta correcta. El problema era que aquesta nova hipòtesi no s'ajustava a les lleis de la física clàssica, havia donat una explicació molt precisa, ni ell mateix creia, era la primera persona que es va prendre seriosament la idea. Albert Einstein va descobrir una cosa que Max Planck no podia creure, la llum no és només una ona contínua que de vegades es comporta com una partícula. Un dels majors èxits intel·lectuals d'Albert Einstein pel qual va obtenir un premi va ser adonar-se que la llum actua com si arribés a fragments, a trossos junts. L'obra d'Einstein va marcar un punt d'inflexió en el desenvolupament de la física moderna. El 1913 Niels Bohr va començar a aportar dades a la teoria quàntica a l'explicar l'estructura de l'àtom i va ser capaç d'explicar les propietats dels àtoms utilitzant la mecànica quàntica. Les matemàtiques de Bohr van mostrar que els electrons no orbitaven al voltant del nucli d'un àtom, com fan els planetes que orbiten al sol, només podien girar al voltant del nucli a certes distàncies concretes. La teoria de Bohr suposava que els electrons es comportaven com partícules. Fins que no va aparèixer el físic francès Louis de Broglie no es va demostrar que les òrbites atòmiques poden explicar suposant que els electrons que normalment es consideren partícules també poden comportar-se com ones. El 1925 Erwin Schrödinger va formular la famosa equació que porta el seu nom, l'equació de Schrödinger, va establir les bases del que va acabar sent una teoria completa de la mecànica quàntica. En definitiva, la teoria quàntica va suposar per als científics el que probablement sigui la teoria més exacte i més potent mai concebuda per la humanitat.
2
II.
Interpretació quàntica de l’àtom
En la física que coneixem tots, tenim molt clar la representació de com és l'àtom, i com hi orbiten els electrons, ja que utilitzem el model atòmic de Bohr per visualitzar-lo. "La cosa és que" aquesta imatge que tenim de l'àtom no representa com són els àtoms realment, més bé l'utilitzem aquest model visual per simplificar i comprendre més fàcilment la física. Aquest model de l'àtom on els electrons giren en una òrbita al voltant del nucli, va ser proposat pel físic Rutherford. Tot i que en el seu moment v a ser un gran descobriment, no es va tardar a trobar-hi problemes, que en aquest cas, va ser la falta d'estabilitat. Per comprendre perquè aquest model no pot correspondre a la realitat, ens imaginem una roda de bicicleta que gira dins de l'aigua. A mesura que va girant, anirà produint petites oscil·lacions en forma onades en l'aigua. A més a més amb el pas del temps el moviment de la roda anirà perdent energia fins a quedar-se en repòs. Doncs bé, una cosa semblant passa amb els electrons de l'àtom de rut herford. A l'estar accelerant-se en un camp electromagnètic, perden energia emesa en forma de llum, procés el qual s'anomena radiació de sincrotró. Que implica això? Doncs que si l'electró va perdent energia, acabarà caient en espiral contra el nucli. És a dir, si els nostres àtoms fossin com els de Rutherford, nosaltres no existiríem. En cerca de la solució a aquest problema, es van presentar diferents models atòmics, però no va ser fins que Schrödinger, presentant la seva creacio matemàtica, que no es va trobar una solució. Quin era el problema en aquesta idea clàssica del model atòmic? Bé, l’electró es troba efectivament girant al voltant de un nucli. La cosa, és que gira de manera quàntica. És a dir, les trajectòries i moviments de l'electró no són les lleis clàssiques a les que estem acostumats, sinó que obeeixen les regles de la mecànica quàntica. Tot això comporta que aquest objecte quàntic experimenti fenòmens com és el de la indeterminació. Això significa que aquest objecte no te perquè estar en un espai concret o tenir una velocitat concreta. I en especial, no te perquè tenir una qualitat de gir concret. Per això la manera correcta de visualitzar l'electró girant, no és a través d'una òrbita que segueix un camí, sinó que la seva posició es troba indefinida en una mena de núvol. Dit tècnicament, és la representació de la funcio d'ona, normalment anomenada orbital. El que ens indiquen els orbitals, és el grau d'indeterminació de la posició que té l'electró en un cert lloc de l'espai. És a dir, la probabilitat la seva creació matemàtica "La funció d'ona" que no es va poder resoldre. Que tenim de trobar-lo en un lloc si el forcem a definir la seva posició. Ja que de normal, la seva posició es troba indeterminada.
3
III.
Experiment de la doble escletxa:
Un dels primers experiments que van demostra l'existència d'una falla en la física clàssica va ser l'experiment de la doble escletxa. Aquest experiment si el pensem conceptualment el podem dividir en 3 parts: - Una màquina de l'atzar, la seva feina simplement és la d'extreure un àtom i col·locar-lo a l'atzar en una de les dues caixes que té connectat. - Les capses són dues caixes normals, amb una obertura lateral que està apuntant a una pantalla detectora. -Una pantalla detectora la qual quan un àtom xoqui contra ella deixarà una marca amb la qual sabrem on ha xocat l'àtom. Per descomptat que l'experiment no és així, però per entendre-ho millor hem tret tota la part tècnica i l'hem simplificat a una cosa conceptual. Els científics van fer el seu primer experiment, però per veure i estudiar el comportament dels àtoms van posar dos detectors, un a cada obertura de cada caixa. En repetir el procediment de tirar àtoms contra la pantalla molts cops seguits van veure que es formava un patró, Aquest patró el podem dividir en dues parts, una concentració d'impactes al davant de cada caixa. Per tant, surten un 50% dels àtoms per cada caixa. Sembla lògic perquè l'àtom no pot sortir de les dues reixes, no? Bé els científics van repetir l'experiment, però van treure els detectors, en fer -ho es van sorprendre, van veure que el patró que sortia era molt diferent de l'esperat. Al principi van pensar que és tractava d'un error i van fer diferents proves, on van ajuntar i separar les caixes i van veure que el patró es mantenia directament proporcional a la distància de les dues caixes. Això els va donar a entendre una cosa bastant sinistra, que és com si l'àtom passes per les dues caixes a la vegada. No que hi hagi dos àtoms ni que l'àtom es parteix en dos. Si no que el mateix àtom estava en els dos llocs al mateix temps. Si l'àtom passa per una de les dues caixes quan surti disparat, ha d'anar amb molta probabilitat a una de les concentracions que es formen, però aquests llocs de la pantalla depenen de la distància entre les caixes. Aquest és el gran problema. Si l'àtom surt d'una caixa no pot portar informació de l'altra caixa, no pot veure's afectat per ella perquè és una caixa en la qual no passa l'àtom, que no intervé de cap manera en aquesta tirada, però la informació arriba a la pantalla, per tant, l'única manera que la separació entre reixes influeixi en el patró és que l'àtom passi per les dues caixes i per tant que l'àtom es trobi en dos llocs diferents a la vegada.
4
En aquest experiment no podem diferenciar si l'impacte s'ha fet des d'una caixa o de l'altre, i molt menys la suma dels trets que ha passat per cada caixa per separat és la que s'obté en l'experiment. Sembla que les dues caixes actuen juntes per crear el patró, i l'única manera que les seves propietats conjuntes es propaguin fins a la pantalla és que l'àtom tingui també aquella informació, per tant, passa a la vegada per les dues reixes. Veiem que quan l'àtom és observat i estudiat per saber com actua, l'experiment crea el patró de les dues concentracions en canvi quan no s'observa genera el que té diverses concentracions. Quan utilitzem els detractors, l'única prova que l'àtom passa per les dues reixes desapareix i en comptes d'això ens surt un patró que ens diu que està en una. És com si el fet de mesurar per quina reixa passa l'àtom fos el que provoques que l'àtom estigues en només una caixa. L'experiment encara té molts dubtes en l'aire, per exemple, com és que l'àtom sembla estar en els dos llocs a la vegada, ens ho hem de prendre literalment? I que hem de veure els observadors en tot això? Que significa exactament mesurar? Siguin les que siguin les respostes, els físics van veure que havien de reinventar-se, que havia de crear una teoria radicalment diferent amb la qual poder manipular-se en aquest estrany món i van crear la mecànica quàntica. Van solucionar el problema que generava l'experiment dient que l'àtom actuava amb la dualitat ona-partícula, quan ens anava bé en algunes situacions era una ona i en altres una partícula. El senyor Broglie va utilitzar aquesta dualitat per entendre les òrbites dels electrons dins de l'àtom de Bohr. I com no, la llum que ja feia un temps que exhibia aquest comportament indecís. Doncs bé, amb aquesta dualitat ona-partícula van poder concloure que l'àtom sortia disparat com una ona i aquesta passava per les dues reixes a la vegada, generant així dues ones les quals quan xoquen contra la pantalla detectora se sumaven en algunes zones i en altres es restaven, i que aquestes zones on se sumaven era els llocs on era més probable que l'ona en xocar es convertís en partícula. I el que passava en posar detectors per veure d'on sortia la partícula era que al detectar l'àtom aquest es transformava a partícula la qual obligaven a l'àtom a estar només en un lloc fent que el seu impacte fos com el d'una bala concentrant -se com en el primer patró que hem vist.
5
IV.
La funció d’ona, la regla de Born i el Principi d’incertesa de Heisenberg.
La dualitat d’ona partícula no reflecteix bé com funciona la quàntica. No podem explicar tota la quàntica simplement pensant en l’electró com una partícula o com una ona. Estem intentant entendre un concepte molt més abstracte i nou amb conceptes clàssics els quals ja entenem. No es tracte d’una partícula que és una ona fins a arribar a un punt que l’interfereix i es converteix en una partícula. Sino que en si la posició que ocuparà l’electró no està determinat, però si que pot tenir més possibilitats a ocupar aquell espai o un altre, si el forcem que ocupi aquell espai. Si d’alguna ona s’hagués de tractar ens l’hauríem d’imaginar com un camp de probabilitats. La funció d’ona i la regla de Born Schrödinger presenta la funció d’ona, es basa en un camp amb valors concrects per a cada punt de l’espai. Ens ho podem imaginar com la temperatura, en que per a punts de l’espai pot tenir valors diferents. Però la funció d’ona ens explica que per a cada punt d’aquests a l’espai hi ha un nombre complex, és a dir, un nombre irreal. Sabem que els nombre complexos es poden expressar en forma de vector. Com a petit recordatori, la part real s’expressa en l’eix de x i l’imaginaria en l’eix de y, així formant un vector.
I és el conjunt de vectors en un espai la que s’anomena funció d’ona,𝚿. Podem determinar una probabilitat cap a on es comportarà la partícula, utilitzant aquest camp de nombre complexos. Born va elevar el valor absolut del mòdul del nombre complex al quadrat, i d’aquest en va obtenir un valor que determinaria la probabilitat que hi havia que la partícula es trobés en aquella posició: |𝑚ò𝑑𝑢𝑙 |2 .Ara el camp de nombre complexos es converteix en un camp de probabilitats, el qual hi ha més probabilitat de trobar l’electró sobre un vector amb mòdul més elevat.
6
A l’experiment de la doble escletxa van trobar més punts en aquells espais amb una probabilitat més gran. Però, què és el que determina com seràn aquests nombre complexos sobre l’espai. L’equació de ona de Schrödinger pot preveure com seràn aquestes probabilitats, però no ens explica el perquè de nombre complexos repartits per l’espai, és a dir, no ens explica el perquè de la funció d’ona. Aquesta resposta no està solucionada encara, però té varies interpretacions.
Cal tenir en compte que és només quan medim l’electró que podem determinar la seva posició en l’espai, mesurar és doncs determinar l’electró, el qual que per si no fos per nosaltres es quedaría en un camp de probabilitats. Tot i així no ho podem saber tot sobre la partícula. Principi d’incertesa de Heisenberg El principi d’incertesa de Heisenberg ens diu que en el mon quàntic no ho podem saber tot sobre l’àtom en total exactitud. Pots saber més o menys sobre la regió on es trobarà l’electró i mes o menys la velocitat que pot tenir. Tanmateix com més precisió tinguis sobre la posició més gran serà la franja de velocitats la qual podría tenir l’electró. I viceversa. Per tant, guanyar exactitud en una quantitat suposa perdre’n en l’altre. Això és degut a que el propi electró no té definides les seves propietats, no perquè no ho sapiguem mesurar. L’electró existeix sense tenir la posició ni la velocitat determinades. Si volgués determinar la posició de l’electró exacta, hauria de totalment indeterminar la velocitat. La funció d’ona seria 0 excepte en un punt. En la mecànica quàntica, aquest és un postulat fonamental i no es refereix únicament a l'error que es produeix en mesurar, sinó a un error intrínsec que no es pot superar.
Webgrafia Max Planck (2019). Recuperado 28 de mayo de 2021, 18:48 de Wikipedia website:
7
https://es.wikipedia.org/wiki/Max_Planck Albert Einstein (2017). Recuperado 28 de mayo de 2021, 19:03 de Wikipedia website: https://es.wikipedia.org/wiki/Albert_Einstein Fig 1: Niels Bohr (2017). Recuperado 28 de mayo de 2021, 19:14 de Wikipedia website: https://es.wikipedia.org/wiki/Niels_Bohr Louis-Victor de Broglie. (2017). Recuperado 28 de mayo de 2021, 19:21 de Wikipedia website: https://es.wikipedia.org/wiki/Louis-Victor_de_Broglie Erwin Schrödinger (2017). Recuperado 28 de mayo de 2021, 19:36 de Wikipedia website: https://es.wikipedia.org/wiki/Erwin_Schr%C3%B6dinger Representació Models atòmics (2018). Recuperado 30 de mayo de 2021 20:36 , de Youtube website: https://www.youtube.com/watch?v=wxIxWTTsBj4 Biografia Niels Bohr (2017). Recuperado 28 de mayo de 2021, 20:40 de buscabiografias. website: https://www.buscabiografias.com/biografia/verDetalle/2081/Niels%20Bohr La Doble Rendija (2017). Recuperado 29 de mayo de 2021, 19:24 https://www.youtube.com/watch?v=Y9ScxCemsPM
de Youtube website:
La doble rendija (2021). Recuperado 29 de mayo de 2021, 22:12 de investigacionyciencia website: https://www.investigacionyciencia.es/blogs/fisica-y-quimica/31/posts/y-elexperimento-de-la-doble-rendija-se-hizo-realidad-11103 La dualidad onda-partícula. (2017). Recuperado 28 de mayo de 2021, 21:49 de Youtube website: https://www.youtube.com/watch?v=LBEq1rhRbC4 Dualidad onda-partícula. (2014). Recuperado 28 de mayo de 2021, 21:30 de Youtube website: https://www.youtube.com/watch?v=nX4ZrC4q_cw&t=183s La física cuántica (2018). Recuperado 30 de mayo de 2021, 20:43 de Nuevarevista website: https://www.nuevarevista.net/el-descubrimiento-de-la-fisica-cuantica Descubrimientos de la física cuántica (2021). Recuperado 29 de mayo de 2021, 22:12 de Granmisterio website: https://granmisterio.org/2014/06/18/descubrimientos-asombrososde-la-fisica-cuantica/ El gato de Shrödinger (2018). Recuperado 27 de mayo de 2021, 20:37 de Youtube website: https://www.youtube.com/watch?v=9JlOmEEyTOU El Principio de Incertidumbre (2018). Recuperado 27 de mayo de 2021, 21:37 de Youtube website: https://www.youtube.com/watch?v=2W8i-BVWehc&t=189s Interpretaciones de la mecánica cuántica (2020). Recuperado 29 de mayo de 2021, 20:14 de Wikipedia website:
8
https://es.wikipedia.org/wiki/Interpretaciones_de_la_mec%C3%A1nica_cu%C3%A1ntica#El _problema_de_la_medida
9...
Similar Free PDFs
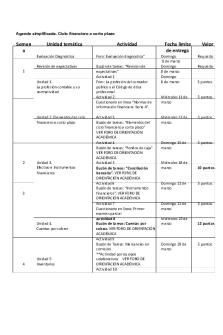
Agenda simplificada
- 3 Pages

Tramitacion Simplificada PAC
- 2 Pages

TA 0521 1+Simplificada+(V9)
- 3 Pages

Física quàntica simplificada
- 10 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu









