Tabla periódica y propiedades periódicas PDF

| Title | Tabla periódica y propiedades periódicas |
|---|---|
| Course | Quimica |
| Institution | Instituto Tecnológico de Tlalnepantla |
| Pages | 4 |
| File Size | 575.9 KB |
| File Type | |
| Total Downloads | 56 |
| Total Views | 130 |
Summary
apuntes de quimica...
Description
REPORTE DEL LABORATORIO DE QUIMICA
GRUPO: K-11 05/05/2020
PROYECTO DE LABORATORIO JOSE DE JESUS CUEVAS VIRUETE
Tabla periódica y propiedades periódicas. El objetivo de la presente práctica de laboratorio es realizar un estudio experimental de la Ley Periódica de los Elementos, mediante diversas pruebas químicas y físicas de las Distintas series de elementos de la tabla periódica.
INTRODUCCIÓN: La tabla periódica se ha vuelto tan familiar que forma parte del material didáctico para Cualquier estudiante, más aún para estudiantes de química, medicina e ingeniería. El experimento realizado en el laboratorio usan varios metales los cuales los ponen a alta temperatura para saber cuáles son metales y no metales añadiéndoles agua destilada y algunos colorantes y así saber en base al color obtenido saber si son metales o no metales . Se realiza un experimento para saber la masa del zinc y el volumen del plomo pesándolo en la báscula y llenando la probeta con agua destilada para obtener el volumen final del plomo. Que es el volumen del sólido.
Propiedades de los metales y de los no metales. PROBLEMA: Identificar las propiedades físicas de los metales y no metales Breve introducción: propiedades físicas que diferencian a los metales de los no metales como son: aspecto físico, dureza, maleabilidad ductilidad, disolución, conductividad eléctrica y térmica. Se realiza un experimento donde utilizando yodo, en polvo y un pedazo en forma de roca, azufre, zinc en granalla y en forma de pepita, cobre en forma de lámina, hierro en polvo y en forma de placa, magnesio en tiras, y aluminio. Se utiliza el ácido clorhídrico y un probador de electricidad para saber si tienen conductividad al momento de meter las dos puntas del metal al acido sin tocarse entre si dando como resultado que el: Aluminio: si es conductor de la corriente eléctrica Yodo: no es conductor de corriente eléctrica Hierro: si es conductor de electricidad Magnesio: si es conductor de electricidad Azufre: no es conductor de electricidad
Zinc: el zinc si es conductor de electricidad Cobre: si es conductor de electricidad
Al terminar esa práctica se agrega ácido clorhídrico a los 5 elementos que si fueron conductores de electricidad, se le pone 15 gotas de ácido alas probetas para ver cuando estén liberando al hidrogeno Al agregar el ácido clorítico a cada metal y dejar un rato no mostro reacción alguna....
Similar Free PDFs

Tabla y propiedades de Laplace
- 1 Pages

Tabla Fitte Y Cervini
- 9 Pages
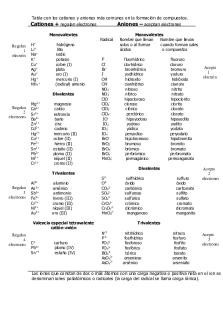
Aniones y cationes tabla
- 1 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu












