Korozja-selektywna - sprawko z korozji selektywnej PDF

| Title | Korozja-selektywna - sprawko z korozji selektywnej |
|---|---|
| Course | Korozja |
| Institution | Politechnika Gdanska |
| Pages | 4 |
| File Size | 331.2 KB |
| File Type | |
| Total Downloads | 51 |
| Total Views | 135 |
Summary
sprawko z korozji selektywnej...
Description
SPRAWOZDANIE Z ZAJĘĆ LABORATORYJNYCH Z PRZEDMIOTU PROCESY KOROZYJNE
Korozja selektywna
Ocena wizualna Po przeszlifowaniu i odtłuszczeniu powierzchni acetonem oceniono barwę elektrod, oraz dokonano pomiaru ich potencjałów względem elektrody NEK.
Materiał
Potencjał [V]
Obserwacje
M63 M60 Cu Zn Y X M59 B101 BA1055
-0,156 -0,127 -0,088 -0,910 -0,117 -0,100
MC70
-0,210
Kolor złotawy Kolor srebrny ze złotym połyskiem Kolor miedziany Kolor srebrny z połyskiem Kolor złotawy, mały połysk Kolor miedziany, mały połysk Kolor jasnozłoty Kolor złoty z czerwonymi przebarwieniami Kolor bardzo jasnozłoty o srebrowym połysku Kolor jasnożółty, widoczny połysk
-0,143
Badania elektrochemiczne
Wywoływanie korozji selektywnej poprzez polaryzację w środowisku 1 % NaCl Dokonano pomiaru potencjału stacjonarnego stopów miedzi względem elektrody odniesienia NEK przy pomocy miernika uniwersalnego. Zauważono, że po zanurzeniu w roztworze próbka zmieniła barwę na ciemniejszą (na krańcach elektrody). Zaobserwowano zmętnienie roztworu i wydzielanie wodoru na elektrodzie pomocniczej. Po kilku minutach elektroda pokryła się łatwościeralnym osadem. Fakt, iż korozja rozpoczęła się od zewnętrznych obszarów anody jest ściśle związany z technologicznym procesem obróbki badanego materiału. Pręt, z którego zbudowana jest elektroda został wyprodukowany za pomocą ciągnienia materiału. Wysokie ciśnienie i temperatura spowodowały zniszczenie struktury krystalograficznej w zewnętrznych obszarach pręta, co sprzyja szybszej korozji. 2H2O + Zn2+ → 2H+ + Zn(OH)2 Proces anodowy: Zn → Zn2+ + 2e-
Proces katodowy: 2H+ + 2e- → H2
Pomiar potencjostatyczny dla stopu M60 w układzie trójelektrodowym. Wykonano pomiar potencjostatyczny dla stopu M60 w układzie trójelektrodowym (WE – elektroda pracująca, CE – przeciw elektroda, RE – elektroda referencyjna) z elektrodą
2
odniesienia NEK w środowisku NaCl z dodatkiem wody amoniakalnej (300ml NaCl + 100ml NH4 · H2O) z polaryzacją +800mV Elektroda pokryła się barwnym kompleksem amonomiedzianowym, który jest łatwościeralny. Zaobserwowano wyraźne zmniejszenie wydzielania wodoru względem badania poprzedzającego. Pomiar elektrody wykonanej z miedzi w środowisku elektrolitycznym z dodatkiem wody amoniakalnej W CuSO4 0,5M z dodatkiem wody amoniakalnej umieszczono elektrodę wykonaną z mosiądzu M63. Polaryzację ustalono na +800mV. Po około minucie można było zaobserwować powstawanie szafirowego kompleksu kationów amonomiedzianowych. Zmiana barwy roztworu jest dobrym wskaźnikiem postępu reakcji. +¿ Cu2+ + 2NH3 × H2O → Cu(OH)2 + 2N H ¿ 4 Cu2+ + OH -- → Cu(OH)2 Cu(OH)2 + 4NH3 × H2O → [Cu(NH3)4](OH)2 + 4H2O Wnioski Na podstawie przeprowadzonych badań stwierdzono, iż:
Próbka X jest wykonana z miedzi Próbka Y jest wykonana z mosiądzu z procentową zawartością Cu między 60%, a 70%
Wpływ dodatków na potencjał
Podstawy technologii maszyn: podręcznik Autor Józef Zawora str.90 wydanie piąte
3
Dodatki do miedzi wpływające negatywnie: P As Si Powodują duże, zniekształcenia i wprowadzają duże naprężenia w sieci krystalicznej Dodatki wpływające na przewodność w stopniu nieznacznym: Powodujące małe zniekształcenia sieci krystalicznej Ag Cd Niewbudowujące się w sieć krystaliczną miedzi: Metale nierozpuszczające się w miedzi Pb Bi Niemetale tworzące wtrącenia w strukturze, które są odizolowane: Tlenki Krzemiany Siarczki
4...
Similar Free PDFs

Sprawko procesy 4 z całkami
- 6 Pages

Termistor - sprawko
- 12 Pages

Sprawko 1 - Stopień: B
- 6 Pages

Sprawko Prostowniki - Grade: 3
- 20 Pages

05 290320 162194 02 - sprawko
- 3 Pages

Z-table - Z chart
- 1 Pages

Z-tabel - Z-tabel
- 3 Pages

Z tables - Z table
- 2 Pages
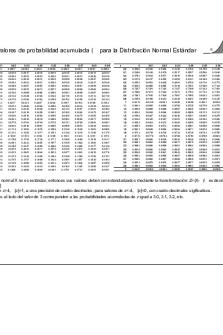
Tabla-z - Tabla Z
- 1 Pages

Notatki z wykładów z bmz
- 19 Pages

Tabla-z - tabla de z
- 1 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu




