TEMA 16. Diabetes mellitus tipo 1 PDF

| Title | TEMA 16. Diabetes mellitus tipo 1 |
|---|---|
| Author | Ainhoa Rubio Lavado |
| Course | Endocrinología y Nutrición Clínica |
| Institution | Universidad de Extremadura |
| Pages | 7 |
| File Size | 267.9 KB |
| File Type | |
| Total Downloads | 748 |
| Total Views | 788 |
Summary
TEMA 16 DIABETES MELLITUS TIPO 1La insulina es una hormona polipeptídica compuesta por 51 aminoácidos, estructurados en dos cadenas, una cadena alfa de 21 aminoácidos y una cadena beta de 30 aminoácidos, ambas unidas por dos puentes disulfuro. Además, en la cadena alfa existe un tercer puede disulfu...
Description
TEMA 16
DIABETES MELLITUS TIPO 1
La insulina es una hormona polipeptídica compuesta por 51 aminoácidos, estructurados en dos cadenas, una cadena alfa de 21 aminoácidos y una cadena beta de 30 aminoácidos, ambas unidas por dos puentes disulfuro. Además, en la cadena alfa existe un tercer puede disulfuro, entre los aminoácidos 6 y 11. Tiene un precursor, denominado proinsulina. La escisión de proinsulina en insulina, y péptido de unión o péptido C se realiza dentro de los mismos gránulos de secreción, por lo que la insulina y el péptido C se liberan en cantidades equimoleculares. La insulina y el péptido C pasan a la vena porta y llegan al hígado . Un porcentaje variable de insulina, entre el 60-80%, ejerce su acción en el hígado, y allí es degradada, de tal forma que por las venas suprahepáticas solo sale entre el 20-40% de la insulina liberada por la célula beta. El péptido C, sin embargo, carente de cualquier acción biológica conocida, atraviesa el hígado sin ser degradado, y prácticamente el 100% pasa a la circulación general. Esto hace que los niveles de péptido C curiosamente sean más demostrativos de la actividad de las células beta que los propios niveles de insulina. La célula beta forma parte de una estructura más compleja, que es el islote de Langerhans . Los islotes se encuentran dispersos entre el páncreas exocrino, y constituyen en peso el 2% aproximadamente del total del páncreas. Los islotes están constituidos por: — Células alfa: Productoras de glucagón. — Células beta: Productoras de insulina. — Células delta: Productoras de somatostatina. — Células pp: Productoras de polipéptido pancreático. — Células productoras de ghrelina. Todas estas células tienen una influencia mutua notoriamente compleja por conexiones vasculares, nerviosas y paracrinas. Las funciones clave de la insulina son: Estimulación de la captación de glucosa desde la circulación sistémica: La entrada de la glucosa en las células se realiza mediante unos transportadores denominados GLUT. Aunque hay siete isoformas diferentes (GLUT 1-7), el más importante para nosotros es el GLUT, ya que es el transportador de la mayoría de la glucosa en los tejidos sensibles a la insulina, incluyendo el músculo esquelético y el tejido adiposo. En la propia célula beta se encuentra el GLUT 2 que contribuye a la regulación de la secreción de insulina. Supresión de la neoglucogénesis hepática. Con estas acciones la insulina regula la homeostasis corporal de la glucosa. Existe un conjunto de hormonas que se oponen al efecto de la insulina que actúan coordinadamente, denominadas las hormonas contrarreguladoras que son, por orden de importancia, el glucagón, las catecolaminas, el cortisol y la hormona del crecimiento. 1
DIABETES MELLITUS:
La diabetes mellitus es una enfermedad caracterizada por la hiperglucemia y otras profundas alteraciones del metabolismo intermediario producida por un déficit, absoluto o relativo, de insulina o por falta de acción de ésta (resistencia a la insulina). La diabetes mellitus se puede clasificar en varios tipos: Diabetes mellitus tipo 1: Caracterizada por un déficit de insulina, o insulinopenia absoluto. A su vez, se divide en dos tipos: — Diabetes mellitus tipo 1A: Se caracteriza por la presencia de anticuerpos contra las células beta. Es abrumadoramente más frecuente. — Diabetes mellitus tipo 1B: Los anticuerpos están ausentes. Diabetes mellitus tipo 2: Es una diabetes definida negativamente, ya que tiene una etiología desconocida, en la que no se detectan anticuerpos contra las células beta. La insulina puede estar, en un momento dado: alta, normal o baja en valores absolutos, pero siempre inferior a la correspondiente para el valor de glucosa. Diabetes gestacional: El embarazo es fisiológicamente diabetógeno, debido a la fabricación de la placenta por hormonas que se oponen al efecto de la insulina (gonadotrofina coriónica, lactógeno placentario…). Por ello durante la gestación, la célula beta se ve impelida a aumentar la síntesis de insulina para compensar la insulinorresistencia del embarazo. Cuando la célula beta es capaz de hacer ese sobresfuerzo, la glucosa se mantiene normal. Cuando es incapaz, aparece una reserva pancreática perfecta de las que no la tienen. Por ello, el haber tenido una diabetes gestacional previa es un factor de riesgo para presentar una diabetes mellitus tipo 2 en el futuro. Entre los factores de riesgo de padecer una diabetes gestacional, tenemos: — Obesidad: A mayor IMC, más probabilidad. — Edad: Se incrementa notablemente por encima de los 30 años. — Antecedentes familiares de diabetes mellitus tipo 2. Diabetes secundaria: Se trata de un factor exógeno que actúa con respecto al metabolismo glucídico. Entre estos factores exógenos, tenemos: — Pancreatectomía: Reduce drásticamente el número de células beta. — Algunas enfermedades endocrinas: Especialmente aquellas que cursan con niveles aumentados de hormonas contrarreguladoras como las catecolaminas (feocromocitoma), GH (acromegalia), glucagón (glucagonoma) o cortisol (S. de Cushing). — Exceso de inhibidores de la insulina (somatostatina). — Ingesta de algunos fármacos: Nuevamente los glucocorticoides. Diabetes monogénica: Está caracterizada por un descenso de la secreción de insulina por la célula beta, causada por una única mutación. Comprende un grupo heterogéneo de diabetes, incluyendo la diabetes neonatal permanente, la diabetes mitocondrial y la diabetes como la del adulto que aparece en la infancia o diabetes tipo MODY. La MODY es la forma más común de diabetes monogénica, con la
2
transmisión autosómica dominante de un gen que codifica un defecto primario de secreción de insulina. Aproximadamente un 2% de la diabetes en Europa es de tipo MODY. Las características clínicas de los pacientes son muy heterogéneas, lo que hace que frecuentemente sean diagnosticados de diabetes mellitus tipo 1 o tipo 2. Existen unos antecedentes de diabetes prominentes (abuelos, padres, hijos…) siempre presentes, la hiperglucemia es moderada con una tendencia mínima a la cetosis antes de la edad de los 25 años, la secreción de insulina en respuesta la sobrecarga oral o intravenosa de glucosa está ligeramente disminuida, y los anticuerpos anticélulas beta están ausentes. Hay actualmente descritos 11 tipos de diabetes tipo MODY, siendo los más frecuentes la MODY 2 con un defecto en el gen de la glucoquinasa y la MODY 3 con un defecto en el gen del factor nuclear hepatocitario 1 alfa (HNF-1a).
NORMALIDAD PARA EL METABOLISMO HIDROCARBONADO:
Para mantener la glucemia normal en todo momento, una persona necesita: Mantener una insulinemia basal: Niveles fisiológicamente bajos de insulina pero que no desaparecen nunca, con los cuales fundamentalmente se regula la lipolisis y el catabolismo proteico , necesarios para mantener una glucemia normal en ayunas, apoyada por la neoglucogénesis hepática, o síntesis de glucosa de novo a partir de ácidos grasos libres (lipolisis) y de aminoácidos (fundamentalmente musculares, como la alanina, procedentes del catabolismo proteico). La insulina basal controla la lipolisis, la destrucción proteica y la propia neoglucogénesis. Tras las comidas: Unos picos de insulina, niveles elevados y cortos, que se encargan de organizar el aluvión de principios inmediatos que llegan al organismo después de una comida. La glucosa es introducida en las células para la alimentación, es almacenada en el hígado (glucogénesis) así como en otros órganos (fundamentalmente el sistema muscular). Con respecto a los aminoácidos, se favorece la síntesis de proteínas (anabolismo proteico) y los triglicéridos se introducen en los adipocitos (lipogénesis). En general, podemos decir que la insulina basal regula la producción de glucosa (neoglucogénesis), mientras que los picos postpandriales de insulina regulan el consumo (captación periférica de glucosa). Con estos conceptos podemos decir que un paciente tiene un metabolismo hidrocarbonado normal cuando tiene: — Glucemia basal inferior a 100mg: Se llama glucemia basal a la que presenta un paciente por las mañanas después de 8 horas de ayuno . A pesar de la facilidad de su medida se correlaciona perfectamente con la neoglucogénesis nocturna. Es decir, una glucemia normal presupone una neoglucogénesis perfectamente regulada por insulinemia basal adecuada. — Glucemia a las dos horas de tomar 75 gramos de glucosa inferior a 140mg: Sobrecarga oral de glucosa, sirve para ver cómo se comporta el organismo ante afluencias masivas de hidratos de carbono, en todas las personas se hace con 75 gramos , menos en niños, que se hace en función del peso, y en embarazadas, en las que se hace con 100 gramos. Esto supone que la glucosa oral ha sido 3
capaz de producir en el páncreas la liberación de un pico de insulina adecuado para permitir su distribución fisiológica por todo el organismo (captación celular, almacenamiento hepático y muscular). — Hemoglobina glucosilada (HbA1c) inferior a 5’7%: La base de este proceso es que todas las proteínas se glicosilan en contacto con glucosa. El porcentaje de glicosilación dependerá del tiempo de exposición y de los niveles de glucemia. Podría medirse el grado de glicosilación de cualquier proteína, aunque se ha optado por comodidad por la Hb, que es fácil de obtener y tiene una vida media de 120 días. Por ello, la HbA1c, es decir, el porcentaje de hemoglobina sérica que ha incorporado glucosa a su molécula, nos indica cual ha sido el nivel medio de glucosa de los últimos 3 meses.
DIAGNÓSTICO DE LA DIABETES MELLITUS:
Un paciente puede ser diagnosticado de diabetes de varias formas: 1. Una glucemia al azar superior a 200mg acompañada de síntomas inequívocos de hiperglucemia: Como poliuria, polidipsia, nicturia, pérdida de peso, polifagia. Lo que estamos diagnosticando aquí es un déficit severo de insulina, es decir, una insulinopenia muy acusada, por lo que en general suelen presentarse así especialmente los diabéticos tipo 1 desconocidos hasta el momento. 2. Dos glucemias basales por encima de 126mg: Es decir, una neoglucogénesis nocturna no regulada por la insulinemia basal, lo que hace que esté ligeramente incrementada con una glucemia basal elevada. 3. Una glucemia a las dos horas de tomar 75 gramos de glucosa superior a 200mg: Esto quiere decir que la glucosa no ha podido ser adecuadamente distribuida por un pico insuficiente de insulina inducido por la sobrecarga. 4. Una HbA1c superior a 6’4%: La determinación puntual de HbA1c da información acerca de la glucosa media de los últimos tres meses antes de la prueba. Una media por encima de 6’4% confirma una glucosa media por encima de los valores determinados para la diabetes. Es una determinación de gran utilidad, ya que no solamente sirve para el diagnóstico, sino que orienta al tratamiento , quien lo necesita y más o menos cual debería ser. Al ser una media no nos informa de cuando está más alta la glucosa, si es en ayunas o postpandrial. 5. La diabetes gestacional tiene sus propios criterios diagnósticos: Normalmente a todas las embarazadas se les realiza un test de screening entre las 24-26 semanas de gestación . Este test de screening, también llamado test de O’Sullivan, consiste en la administración de 5 gramos de glucosa a cualquier hora del día, sin necesidad de que el paciente esté en ayunas. Es normal un valor de menos de 140mg a la hora de la ingesta. Las mujeres que den más de esta cifra deberán someterse a una sobrecarga oral de glucosa con 100 gramos, siendo los valores normales los siguientes: — Basal < 95mg.
— Dos horas < 155mg.
— Una hora < 180mg.
— Tres horas < 140mg. 4
ESTADOS INTERMEDIOS: Los estados intermedios a veces también llamados prediabetes, serían aquellos en las que las cifras de glucosa no son normales, pero tampoco alcanzan aquellas que son diagnosticadas de diabetes. Existen tres estadios intermedios: — Glucemia basal alterada: Son aquellos sujetos que tienen glucemias basales entre 100 y 126 mg. — Intolerancia a los hidratos de carbono: Está presenta cuando a las dos horas de 75 gramos de glucosa por vía oral la glucemia está entre 140 y 200 mg. — HbA1c entre 5’7 y 6’4%.
DIABETES MELLITUS TIPO 1: Se conoce como diabetes tipo 1 a la diabetes autoinmune. En España hay, aproximadamente, 15 diabéticos por cada 100.000 habitantes menores de 30 años. La DM tipo 1 tiene una distribución mundial muy evidente, de forma que cuando más lejos está un país del círculo polar , mayor incidencia, de forma que el país con mayor incidencia de DM tipo 1 es Finlandia. Además, los casos no se presentan de forma uniforme durante todo el año, de forma que hay menos casos en verano y más casos en invierno. La historia natural de un diabético tipo 1 sería un paciente que nace con una cantidad de células beta normales, pero con una predisposición genética hacia la enfermedad . La disposición genética no indica enfermedad, es decir, no por nacer con predisposición se tiene diabetes tipo 1. Casi todos los diabéticos, en la cadena DQ, son DQ301 o DQ501. Además, los diabéticos en general no tienen el ácido aspártico en el aa57 de la cadena DQB. Esta posición, en los HLA, es una posición vital, de forma que es la posición que enseña los antígenos al sistema inmunitario. Los pacientes susceptibles, por tanto, son DQ301, DQ501 o no tienen el ácido aspártico en la cadena DQβ. El desencadenante de la enfermedad no es uno, sino que son varios, como los virus. Es algo inocuo, de forma que está en contacto con todo el mundo, y solo afecta a los que tienen la predisposición. Además de los virus, tenemos otros agentes, como algunos agentes químicos, como pesticidas o raticidas. Una vez que se pone en contacto con el desencadenante, el número de células β comienza a disminuir, además de que se pueden detectar en sangre anticuerpos contra las células β. Anticuerpos contra las células β hay muchos, como los ICA, ICSA, AntiGAD, Antiinsulina, AntiA2… De todos ellos, probablemente el más útil es el AntiGAD. Los anticuerpos son marcadores de la respuesta autoinmune, pero son inocuos, es decir, no tienen la capacidad de destruir a la célula β, sino que lo que destruye realmente a la célula β son los linfocitos T activados.
5
Van muriendo más células β, de forma que cuando se han destruido el 90% de las células β, la glucosa, que se había mantenido en este periodo, comienza a aumentar, comenzando el periodo de la hiperglucemia. La fase de hiperglucemia es asintomática. La glucemia, una vez que llega a un cierto umbral, comienza a dar síntomas. Estos síntomas son poliuria (y nicturia), polidipsia, pérdida de peso y polifagia (las 4P). La poliuria es debida a que, en el riñón, el umbral de glucosa (alrededor de 140) no permite reabsorber más glucosa, por lo que pasa a orina, que arrastra agua por su poder osmótico, produciéndose una diuresis osmótica. Así, el individuo presenta glucosuria. A mayor glucosuria, mayor diuresis osmótica y, por tanto, mayor poliuria. Esta poliuria produce el reflejo de la sed , produciendo a su vez polidipsia. Además, como la poliuria es igual de día que de noche, aparece también la nicturia. La pérdida de peso es debida, fundamentalmente, a que la insulina es la llave que permite que la glucosa se introduzca dentro de las células. Si la glucosa se queda fuera de las células porque no está presenta la insulina, las células no pueden tomar nutrientes, perdiéndose peso. No todos los tejidos dependen de la insulina para tomar glucosa, como el tejido nervioso , pero el tejido muscular, tejido adiposo y el músculo cardíaco sí requieren de insulina. Al perder peso, aparece mayor cantidad de hambre, por lo que se presenta la polifagia, aumentando aún más la hiperglucemia. La diabetes tipo 1 tiene dos tipos de incidencia en la vida: uno alrededor de los 10-12 años y otro a los 30 años. Si los síntomas son ignorados y la enfermedad sigue progresando, se produce una lipolisis por falta de insulina (la insulina es lipogénica). Los ácidos grasos libres pasan a circulación, y se metabolizan en el hígado para producir energía. Los ácidos grasos libres produce cuerpos cetónicos, radicales ácidos que producen una acidosis metabólica. La acidosis metabólica se intenta compensar con una alcalosis respiratoria, con una respiración rápida de Kussmaul, cuyo objetivo es disminuir el CO2. Con este proceso, se produce una cetoacidosis diabética, que es una descompensación aguda extrema de un diabético tipo 1, insulinopénico con una poliuria extrema, deshidratado y caquéxico. Si el pH es menor de 7, ya la cetoacidosis es muy grave. Un paciente que llega a urgencias con cetoacidosis, se estima que ha perdido 6 litros de agua aproximadamente, tendrá una glucosa alta (entre 250-350), con un potasio alto, normal o bajo, y una cetonemia mayor de 0’3 . El tratamiento de la cetoacidosis diabética se basa en la administración de lo que al paciente le falta. 1. Se administran líquidos: Que son casi tan importantes como la propia insulina Se administra, en general, unos 8 litros en 24 horas , de más a menos. Normalmente, se utiliza suero fisiológico, que tiene 143 mEq de sodio por litro y 143 mEq de CI por litro. 2. Hay que administrar insulina por bomba: La insulina en una dosis de 6 unidades por hora es suficiente para saturar los receptores.
6
3. Falta el potasio: El potasio, en un niño de 10-12 años se puede poner sin problemas, pero hay que controlar si el paciente orina bien. En cuanto orine bien, se pude poner sin problema. Se suele añadir 20 mEq de KCl en cada medio litro de suero. 4. Se da bicarbonato: Nunca se debe dar en una cetoacidosis diabética a no ser que el pH esté por debajo de 7, es decir, que el pH sea un problema. En caso de que no, con la administración de suero, insulina y potasio el pH se vuelve a niveles normales. El déficit de bicarbonato se calcula mediante la siguiente
fórmula:
Una vez que tenemos el déficit, administramos un tercio del déficit. La mortalidad de la cetoacidosis diabética es muy baja, ya que el tratamiento es muy simple. La única complicación que está descrita en el tratamiento es la muerte por edema cerebral, que no se sabe si es debido al tratamiento o a la propia cetoacidosis. Se cree que es debido a cambios bruscos de pH en la BHE.
7...
Similar Free PDFs

Caso diabetes mellitus tipo 2
- 7 Pages

Diabetes Mellitus TIPO 2- Place-MAY
- 37 Pages

Diabetes mellitus
- 15 Pages

Diabetes Mellitus
- 3 Pages

Diagnosis Diabetes Mellitus
- 4 Pages
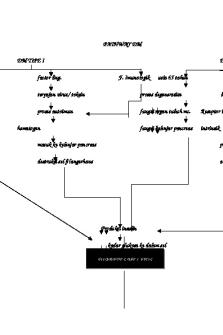
Pathway of Diabetes Mellitus
- 4 Pages

makalah diabetes mellitus
- 10 Pages

DIABETES MELLITUS RESÚMEN CLAVE
- 3 Pages

PAE diabetes mellitus
- 16 Pages

Diabetes Mellitus em gatos
- 8 Pages

Ensayo diabetes mellitus
- 3 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu




