metodos de preparacion y uso de disoluciones patron oxidorreducciones PDF

| Title | metodos de preparacion y uso de disoluciones patron oxidorreducciones |
|---|---|
| Author | veronica rivera |
| Course | Métodos Cuantitativos |
| Institution | Instituto Politécnico Nacional |
| Pages | 8 |
| File Size | 324.1 KB |
| File Type | |
| Total Downloads | 416 |
| Total Views | 647 |
Summary
Instituto Politécnico NacionalUnidad Profesional Interdisciplinaria de BiotecnologíaPRÁCTICA N°PREPARACIÓN Y USO DE DISOLUCIONESPATRÓN OXIDOREDUCTORASLaboratorio de Métodos CuantitativosEquipo:INTEGRANTES: Vásq...
Description
! ! ! ! ! Instituto!Politécnico!Nacional! Unidad!Profesional!Interdisciplinaria!de!Biotecnología! !
PRÁCTICA(N°(3! !
PREPARACIÓN(Y(USO(DE(DISOLUCIONES( PATRÓN(OXIDOREDUCTORAS( !
Laboratorio!de!Métodos!Cuantitativos! !
Equipo:!5! ! INTEGRANTES:! ! •! Vásquez!Ramírez!Linda!Ivett! •! Pacheco!Castillo!Minel! •! Rivera!Cruz!Verónica! ! PROFESORAS:! !
•! Aguilar!Doroteo!Leticia! •! Emma!Bolaños!Valerio!! ! GRUPO:!!2LM2! ! ! ! ! ! ! ! ! !
Fecha(de(entrega:!16!de!Marzo!del!2021.!
1.! OBJETIVOS.! ! a.! Preparar!y!estandarizar!una!disolución!de!KMnO4.!! b.! Preparar!y!estandarizar!una!disolución!de!Na2S2O3.!! ! 2.! INTRODUCCIÓN! ! La!definición!de!Arrhenius!de!ácidos!y!bases!son!limitadas!en!el!sentido!de!que!sólo! se! aplican! a! disoluciones! acuosas.! En! 1932,! el! químico! danés! Johannes! Bronsted,! propuso! una! definición! más! amplia! de! ácidos! y! base! que! no! requiere! que! estén! en! disolución!acuosa.!Un!ácido!es!un!donador!de!protones,!y!una!base!de!Bronsted!es!un! receptor!(Chang,!2002).! Las! reacciones! de! oxidación^reducción! o! redox! son! aquellas! en! que! se! transfieren! electrones!de!un!átomo,!ión!o!molécula.!La!oxidación!es!el!proceso!en!que!un!átomo,!ión! o! molécula! pierde! uno! o! más! electrones;;! la! reducción! implica! ganancia! de! uno! o! más! electrones!por!parte!de!un!átomo,!ion!o!molécula.!Un!agente!reductor!es!una!sustancia! que!pierde!uno!o!más!electrones!y!en!este!proceso,!se!oxida;;!por!otra!parte,!un!agente! oxidante!gana!uno!o!más!electrones!y!con!ello!se!reduce.!Dicho!de!otra!forma,!un!reductor! es!un!donador!de!electrones!y!un!oxidante!es!un!receptor!de!electrones.!! Las!reacciones!de!oxidación^reducción!forman!una!parte!importante!del!mundo!que! nos!rodea.!Abarca!desde!la!combustión!de!los!combustibles!fósiles!hasta!la!acción!de!los! blanqueadores!domésticos,!reacciones!en!la!industria!de!alimentos.!Asimismo,!la!mayoría! de! los! elementos! metálicos! y! no! metálicos! se! obtienen! a! partir! de! sus! minerales! por! procesos! de! oxidación! y! reducción.! Muchas! reacciones! redox! importantes! se! llevan! a! cabo!en!agua!pero!no!implica!que!todas!las!reacciones!redox!sucedan!en!medio!acuoso! (Chang,!2002).! La! aplicación! del! permanganato! en! los! procesos! de! titulación! es! muy! importante! debido!a!que!es!un!oxidante!muy!fuerte!y!su!color!púrpura!intenso!es!suficiente!para!servir! de!indicador!en!la!mayoría!de!las!titulaciones,!se!utiliza!en!disolución!ácida!dando!Mn!(II)! como!producto!de!su!reducción,!en!algunas!aplicaciones!se!realiza!en!medio!casi!neutro! o!incluso!alcalino,!dando!MnO2!como!producto!de!reducción.!! En!esta!práctica!se!empleó!permanganato!de!potasio!(KmnO4)!como!indicador!gracias! a!su!intenso!color!violeta!azulado!y!a!su!vez!como!el!agente!oxidante,!puede!almacenarse! en!recipientes!cerrados!en!frío,!en!áreas!secas!sobre!piso!de!concreto!y!debe!protegerse! del! daño! físico,! se! emplean! frascos! color! ámbar! para! evitar! la! acción! de! la! luz! y! la! contaminación! del! polvillo! atmosférico,! como! sabemos,! en! disoluciones! neutras! o! ligeramente! alcalinas! y! en! ausencia! de! luz,! la! descomposición! es! tan! lenta! que! no! se! puede! medir,! pero! la! luz! actúa! como! catalizador! por! lo! que! no! debemos! usar! frascos! transparentes!para!almacenar!permanganatos.!! Las! titulaciones!con!el!permanganato!de!potasio!deben! llevarse!a!temperaturas!de! entre!60^70ºC,!pues!a!temperaturas!bajas!la!reacción!es!muy!lenta,!ya!en!ebullición!se! potencializa!la!descomposición!del!H2C2O4!en!CO2!y!H2O.! ! ! 3.! MATERIALES!Y!REACTIVOS!
( •! •! •! •!
1!vaso!de!precipitados!de!250!mL! 1!vaso!de!precipitados!de!150!mL!!! 4!vasos!de!precipitados!de!100!mL! 2!matraces!volumétricos!de!100!mL!
•! •! •! •! •! •! •! •! •! •! •! •! •! •! •! •! •! •!
1!bureta!de!25mL! 1!probeta!de!100!mL! 1!pipeta!volumétrica!de!5!mL! 1!pipeta!graduada!de!10!mL! 1!pipeta!graduada!de!1!Ml! 1!termómetro! 1!pinza!para!bureta! 1!soporte!universal! 1!parrilla!de!calentamiento! 1!placa!de!agitación! 1!agitador!magnético! Disolución!de!KMnO4!0.02M! Disolución!de!Na2S2O3!0.07!M! Disolución!de!H2SO4!2.5M! Disolución!de!almidón!al!0.1%!en!peso! Yoduro!de!potasio! Oxalato!de!sodio! Yodato!de!potasio!
! 4.! DIAGRAMAS!DE!FLUJO!! ! a.! Disoluciones.! i.! Disolución!de!KMnO4!0.02!M.!!
! ii.! Disolución!de!Na2S2O3!0.07!M.!
!! iii.! Disolución!de!H2SO4!2.5!M.!!
iv.! Indicador!de!almidón!al!0.1%!(W/V).! !
b.! Estandarización!de!una!disolución!de!KMnO4!0.02!M.!(Por!triplicado).!
! !
c.! Estandarización!de!una!disolución!de!Na2S2O3!0.07!M.!(Por!triplicado).!
! ! ! 5.! RESULTADOS!! ! Tabla!1.!Resultados!experimentales!de!ambas!estandarizaciones.!
Repetición)
Peso% Na2C2O4% [g]%%
Vol.%KMnO4% gastados%[mL]%
1" 2" 3"
0.0282% 0.0279% 0.0301%
4.2% 4.2% 4.4%
Peso%KIO3% Vol.%Na2S2O3% [g]% gastados%[mL]% 0.0351% 0.0314% 0.0304%
14% 13.1% 13%
! ! 6.! ANÁLISIS!DE!RESULTADOS! ! a.! Establecer! la! reacción! que! se! verifica! entre! el! oxalato! de! sodio! y! el! permanganato!de!potasio.! ! 10#$ + 16H () + 2MnO$. + 5C1 O1$ → 2Mn1( + 8H1 O + 10CO1 + 10#$ ! ! En!el!siguiente!reacción!ya!se!ha! tomado!en!cuenta!que! se!lleva!en!presencia!de! ácido!sulfúrico:! ! 2𝐾𝑀𝑛𝑂. + 8𝐻1 𝑆𝑂. + 5𝑁𝑎1 𝐶1 𝑂. → ) 2𝑀𝑛𝑆𝑂. + 8𝐻1 𝑂 + 10𝐶𝑂1 + 𝐾1 𝑆𝑂. + 5𝑁𝑎1 𝑆𝑂. ! ! ! b.! Establecer!la!reacción!que!se!verifica!entre!el!yodato!de!potasio!y!el!yoduro! de!potasio!en!medio!ácido.! ! ! KIO? + 5KI + 3H1 SO. → 3I1 + 3K1 SO. + 3H1 O ! c.! Establecer!la!reacción!que!se!verifica!entre!el!yodo!y!el!tiosulfato!de!sodio.!! !
2Na1 S1DD O? + I 1 → 2NaI + Na1 SE/1 1 OG ! d.! Con!los!datos!experimentales!obtenidos,!determinar!la!concentración!exacta! del!permanganato!de!potasio!y!del!tiosulfato!de!sodio.! ! ! !
Tabla!2.!Concentraciones!de!permanganato!de!potasio!y!tiosulfato!de!sodio.!
Repetición)
KMnO4( [mol/L](
Na2S2O3( [mol/L](
1" 2" 3" Promedio""
0.02! 0.0198! 0.0213! 0.0203(
0.0234! 0.0222! 0.0216! 0.0224(
! ! e.! Calculo!de!CV!y!error.!! Se!considera!valor!real!la!molaridad!de!0.02!M!para!el!permanganato!de!potasio!y! de!0.07!M!para!el!tiosulfato!de!sodio.!! !
Tabla!3.!Cálculos!estadísticos.!
)
KMnO4( [mol/L](
Na2S2O3( [mol/L](
Desviación"estándar"
0.00066!
0.00074!
Coeficiente"de"variación"
3.265!
3.340!
%"de"error"respecto"al"valor" real"
1.5%! ^68%! ! 7.! DISCUSIÓN!! Los! resultados! de! ambas! estandarizaciones! rebasa! el! 2%! del! coeficiente! de! variación! que! se! permite,! pero! se! puede! observar! que! en! la! estandarización! de! KMnO4!el!%!de!error!no!es!grande,!atribuimos!el!alto!CV!a!errores!que!se!pudieron! cometer!al!pesar!los!sólidos!o!al!titular.!El!valor!tomado!como!valor!exacto!o!real!fue,! para!el! permanganato! de!potasio,! de!0.02! M,! del!cual! las! concentraciones!no! se! alejan!mucho.!! Por! otro! lado,! para! la! estandarización! del! Na2S2O3,! el! porcentaje! de! error! salió! negativo!dado!que!el!promedio!de!las!concentraciones!obtenidas!es!de!0.0224!M,!y! el!valor! que! se! consideró! real! es! de! 0.07! M! para! el! tiosulfato!de! sodio,! esta! vez! creemos!que! se!debe! a!que! el!valor!real!no! es!de!0.07!M,!ya! que!los!resultados! obtenidos!son!cercanos!entre!sí,!a!menos!que!se!hayan!cometido!grandes!errores! al!momento!de!realizar!el!experimento!o!al!momento!de!balancear!las!ecuaciones! para!sacar!la!estequiometría,!que!se!manejó!como!2:1,!o!realizar!los!cálculos.!El!CV! está!alrededor!del!3%,!lo!cual!también!excede!el!límite!del!2%.!! ! 8.! CONCLUSIONES!! •! Para!la!reacción!de!yodo!con!tiosulfato!de!sodio,!las!propiedades!redox!de! los! iones! tiosulfato! son! bastante! complejas! dada! la! gran! variedad! de! oxoaniones!del!azufre,!la!reacción!suele!producirse!con!el!diyodo.! •! Los! permanganatos! reaccionan! más! rápido! a! altas! temperaturas! y! deben! envasarse!en!frascos!ámbar!para!evitar!la!reacción!con!la!luz.!
•! Es! importante! tener! en! cuenta! la! estequiometría! de! las! reacciones! para! poder!obtener!un!dato!confiable!de!la!concentración!de!una!disolución.!! •! Se!aprendió!teóricamente!a!preparar!las!disoluciones!de!permanganato!y!de! tiosulfato! y! se! analizó! la! reacción! que! se! lleva! en! ambos! casos,! de! igual! forma!se!obtuvieron!las!concentraciones!de!dichos!experimentos.!! ! 9.! MEMORIA!DE!CÁLCULO! ! a.! Para!obtener!la!concentración!de!KMnO4! 𝑚𝑜𝑙𝑒𝑠)𝑁𝑎1 𝐶1 𝑂. = 0.0282𝑔𝑁𝑎1 𝐶1 𝑂. ) ! 2.10𝑥10$. 𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. ! 𝑀RSTUV = !
2𝑚𝑜𝑙𝐾𝑀𝑛𝑂. ) = 8.4𝑥10$E 𝑚𝑜𝑙)𝐾𝑀𝑛𝑂. ! 5𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂.
𝑚𝑜𝑙 8.4𝑥10$E 𝑚𝑜𝑙))𝐾𝑀𝑛 𝑂. = 0.02 ! $? 4.2𝑥10 )𝐿))𝐾𝑀𝑛 𝑂. 𝐿
𝑚𝑜𝑙𝑒𝑠)𝑁𝑎1 𝐶1 𝑂. = 0.0279𝑔𝑁𝑎1 𝐶1 𝑂. ) ! 2.08𝑥10$. 𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. ! 𝑀RSTUV = !
𝑚𝑜𝑙 8.32𝑥10$E 𝑚𝑜𝑙))𝐾𝑀𝑛𝑂. = 0.0198 ! $? 𝐿 4.2𝑥10 )𝐿))𝐾𝑀𝑛 𝑂.
! 2.246𝑥10$. 𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. !
! ! 𝑀RSTUV = !
𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. ) = 2.246𝑥10$. ! 𝑔 134 𝑚𝑜𝑙
2)𝑚𝑜𝑙𝐾𝑀𝑛𝑂. ) = 8.98𝑥10$E 𝑚𝑜𝑙)𝐾𝑀𝑛𝑂. ! 5)𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂.
𝑚𝑜𝑙 8.98𝑥10$E 𝑚𝑜𝑙))𝐾𝑀𝑛𝑂. = 0.0213 ! $? 4.2𝑥10 )𝐿))𝐾𝑀𝑛 𝑂. 𝐿
𝑚𝑜𝑙 0.02 + 0.0198 + 0.0213 𝐿 𝒎𝒐𝒍 ( = 𝟎. 𝟎𝟐𝟎𝟑 𝑳 3
)𝐷𝐸 = ) !
𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. ) = 2.08𝑥10$. ! 𝑔 134 𝑚𝑜𝑙
2)𝑚𝑜𝑙𝐾𝑀𝑛𝑂. ) = 8.32𝑥10$E 𝑚𝑜𝑙)𝐾𝑀𝑛𝑂. ! 5)𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂.
𝑚𝑜𝑙𝑒𝑠)𝑁𝑎1 𝐶1 𝑂. = 0.0301𝑔𝑁𝑎1 𝐶1 𝑂. )
𝑀RSTUV =
𝑚𝑜𝑙𝑁𝑎1 𝐶1 𝑂. ) = 2.10𝑥10$. ! 𝑔 134 𝑚𝑜𝑙
1.33𝑥10$G ∗ = 0.000664! 3
*Es!la!diferencia!de!cada!dato!y!el!promedio!elevado!al!cuadrado![(X^µ)^2]!
𝐶𝑉 = ! %𝐸𝑅𝑅𝑂𝑅 = !
0.000664 = 3.26! 0.0203
0.0203 − 0.02 𝑥100 = 1.5! 0.02
b.! Para!obtener!la!concentración!de!tiosulfato!de!sodio.!! ! 𝑚𝑜𝑙𝑒𝑠)𝐾𝐼𝑂? = 0.0351𝑔𝐾𝐼𝑂? ) ! 1.64𝑥10$. 𝑚𝑜𝑙𝐾𝐼𝑂? ! 𝑀ijklkUm = !
2)𝑚𝑜𝑙𝑁𝑎1 𝑆1 𝑂? ) = 3.28𝑥10$. 𝑚𝑜𝑙)𝑁𝑎1 𝑆1 𝑂? ! 1)𝑚𝑜𝑙𝐾𝐼𝑂?
𝑚𝑜𝑙 3.28𝑥10$. 𝑚𝑜𝑙))𝑁𝑎1 𝑆1 𝑂? ! = 0.0234 𝐿 14𝑥10$? )𝐿))𝑁𝑎1 𝑆1 𝑂?
𝑚𝑜𝑙𝑒𝑠)𝐾𝐼𝑂? = 0.0314𝑔𝐾𝐼𝑂? ) ! 1.46𝑥10$. 𝑚𝑜𝑙𝐾𝐼𝑂? ! ! 𝑀ijklkUm = !
𝑚𝑜𝑙 2.92𝑥10$. 𝑚𝑜𝑙))𝑁𝑎1 𝑆1 𝑂? ! = 0.0222 $? 𝐿 13.1𝑥10 )𝐿))𝑁𝑎1 𝑆1 𝑂?
! 1.42𝑥10$. 𝑚𝑜𝑙𝐾𝐼𝑂?
𝑀ijklkUm = !
𝑚𝑜𝑙𝐾𝐼𝑂? $. 𝑔 ) = 1.46𝑥10 ! 214 𝑚𝑜𝑙
2)𝑚𝑜𝑙𝑁𝑎1 𝑆1 𝑂? ) = 2.92𝑥10$. 𝑚𝑜𝑙)𝑁𝑎1 𝑆1 𝑂? ! 1)𝑚𝑜𝑙𝐾𝐼𝑂?
𝑚𝑜𝑙𝑒𝑠)𝐾𝐼𝑂? = 0.0304𝑔𝐾𝐼𝑂? )
! !
𝑚𝑜𝑙𝐾𝐼𝑂? $. 𝑔 ) = 1.64𝑥10 ! 214 𝑚𝑜𝑙
𝑚𝑜𝑙𝐾𝐼𝑂? $. 𝑔 ) = 1.42𝑥10 ! 214 𝑚𝑜𝑙
2)𝑚𝑜𝑙𝑁𝑎1 𝑆1 𝑂? ) = 2.84𝑥10$. 𝑚𝑜𝑙)𝑁𝑎1 𝑆1 𝑂? ! 1)𝑚𝑜𝑙𝐾𝐼𝑂?
𝑚𝑜𝑙 2.82𝑥10$. 𝑚𝑜𝑙))𝑁𝑎1 𝑆1 𝑂? ! = 0.0216 $? 𝐿 13𝑥10 )𝐿))𝑁𝑎1 𝑆1 𝑂?
0.0216 + 0.0222 + 0.0234 𝑀RSTUV =
3
! )𝐷𝐸 = ) !
𝑚𝑜𝑙 𝐿 = 𝟎. 𝟎𝟐𝟐𝟒 𝒎𝒐𝒍( 𝑳
1.68𝑥10$G ∗ = 0.000748! 3
*Es!la!diferencia!de!cada!dato!y!el!promedio!elevado!al!cuadrado![(X^µ)^2]!
𝐶𝑉 = ! %𝐸𝑅𝑅𝑂𝑅 = !
0.000748 = 3.26! 0.0224
0.0224 − 0.07 𝑥100 = −68! 0.07
! ! 10.!BIBLIOGRAFÍA! ! •! Chang,!R.!(2008).!Fisicoquímica!(3ª!ed.).!E.!U.!A.:!McGraw^Hill,!pp.!405^412! •! Rubinson,!J.!y!Rubinson,!K.!(2000).!Química!analítica!contemporánea!(1ª!ed.).!México:! Pearson.!
!...
Similar Free PDFs

Conceptos de trabajador patron
- 7 Pages

Reporte: Preparación de disoluciones
- 13 Pages

PREPARACION DE PIEL
- 16 Pages
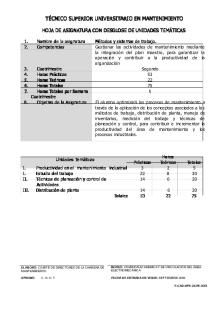
Metodos y Sistemas de Trabajo
- 17 Pages

Generalidades de Disoluciones
- 4 Pages

Uso de nexos y conectores
- 2 Pages

Manual de preparacion de reactivos
- 23 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu








