Biochimie 3 - ATP - Notes de cours 3 PDF

| Title | Biochimie 3 - ATP - Notes de cours 3 |
|---|---|
| Author | Grant Talbot |
| Course | Biochimie |
| Institution | Université Le Havre Normandie |
| Pages | 5 |
| File Size | 283.5 KB |
| File Type | |
| Total Downloads | 56 |
| Total Views | 146 |
Summary
Biochimie 3 - ATP...
Description
Biochimie
I/ La production de l’ATP 1. Contrôle de la synthèse de l’ATP Rappel : 38 moles d’ATP produite / mole de glucose consommée Réaction : ADP + Pi ATP La vitesse effective de la phosphorylation oxydative est imposée par la disponibilité en ADP. Il y aura alors un système de contrôle respiratoire impliquant les électrons. Intérêt : Les électrons ne parcourent la chaine qui si la synthèse de l’ATP est nécessaire ! On distinguera alors 2 cas : Si la [ADP] est forte Si la [ADP] est faible Si la [ADP] est forte : On ajoute de l’ADP à une mitochondrie, alors la vitesse de consommation d’oxygène va s’élever. Ceci est du au fait que des électrons seront transportés le long de la chaine… Lorsque tout l’ADP sera phosphorylé en ATP, la vitesse d’utilisation de l’oxygène sera diminuée. Si la [ADP] est faible : Le taux d’ATP sera élevé Le transport des électrons n’aura pas lieu ! Les coenzymes de type FADH2 et NADH vont s’accumuler La glycolyse et le CK seront inhibés
2. Exportation de l’ATP La membrane mitochondriale renferme plusieurs enzymes spécialisées dans le passage des molécules de part et d’autre. On trouve notamment 2 Perméases qui vont assurer le transport du phosphate ou de l’ADP. Le déplacement va s’effectuer dans le sens d’une entrée dans la matrice mitochondriale pour ces molécules provenant du cytosol. Ce transport va s’effectuer en échange de l’ATP. Rappel : l’ATP est produit dans la mitochondrie par la phosphorylation oxydative Sortie d’ATP L’exportation de l’ATP va nécessiter de l’énergie ! Cette énergie sera fournie par plusieurs phénomènes :
Un gradient de proton H+ : ce procédé est du au mécanisme de pompage de protons. Il va entrainer l’établissement d’un niveau de pH plus faible du côté externe.
La sortie des ions OH-
La combinaison de chaque ion H+ avec un ion OH- pour donner de l’eau
La présence d’un Perméase : o De type antiport o Elle joue un rôle de Translocase de phosphate 1
Biochimie
o o o o
Elle va catalyser un échange entre le phosphate et OHLe pompage de H+ aura permis aux mitochondries d’accumuler le phosphate… Ce phosphate provient du cytosol Ils s’accumule contre un gradient de concentration
L’existence d’un TRANSLOCASE de nucléotide o Elle assure l’entrée de l’ADP o Elle représente 15% des protéines de la membrane interne o ATP/ADP translocase = enzyme-clé o M = 116 000 o Elle contient 4 sous-unités
Elle est située dans une membrane interne mitochondriale. Elle va assurer le transport d’une molécule d’ADP porteuse de 3 charges négatives. En échange d’une molécule d’ATP ayant 4 charges négatives qui va sortir. La vitesse de ce transport de l’ADP vers la matrice (entrée) est l’étape la plus lente de la chaine respiratoire mitochondriale (dans les conditions physiologiques). Cette translocase va contrôler la vitesse de la chaine. Toute diminution du rapport ATP/ADP dans le cytoplasme sera répercutée sur le même rapport dans la matrice. Accélération de la chaine respiratoire
3. Effets des poisons mitochondriale)
métaboliques
sur
la
CRM
(=
chaine
respiratoire
Divers poisons mortels peuvent inhiber la respiration cellulaire… Ils vont perturber la chimiosmose. Ils se répartissent en 2 catégories : Les agents bloquants Les agents découplants
2
Biochimie
a. Les agents bloquants de la CRM Principe : ils vont entraver le flux des électrons le long de la chaine de transport, ce qui aura pour conséquence de bloquer la chaine. Le transport des protons et la synthèse de l’ATP seront empêchés. Exemple : le cyanure CN (le plus puissant) Effet : il interrompt précisément le passage des électrons entre le cytochrome a3 et l’accepteur final O2. b. Les agents découplants de la CRM Principes : ils vont court-circuiter le courant des protons H+. Ils tendant à augmenter la perméabilité de la double couche lipidique aux H+. Conséquence : La chaine va travailler à fond La consommation d’O2 va augmenter La diffusion (fuite) des H+ va annuler le gradient de H+ La synthèse d’ATP sera arrêtée ! L’énergie libérée par la chaine de transport d’électron sera transformée en chaleur. Surchauffe dans les mitochondries Mort cellulaire par excès de chaleur Exemple : 2,4 dinitrophénol (2,4 DNP) Dicoumarol
4. Les navettes membranaires Les différentes étapes de la respiration cellulaire ont produit 2 sortes de coenzymes NADH selon la localisation des évènements. On aura du NADH mitochondrial et du NADH cytosolique. La cellule devra ré-oxyder ces coenzymes. Le but est de régénérer un stock de NAD+ qui pourra à nouveau alimenter la glycolyse. Pour le NADH mitochondrial : Ré-oxydation par le complexe I de la chaine de transport. Ce complexe est accessible par la matrice mitochondriale. Pour le NADH du cytosol : La membrane interne est imperméable. Ce NADH est en provenance de la glycolyse (réaction 6). Solution : Les cellules eucaryotes utilisent des systèmes de navettes. Elles vont transférer les électrons provenant du NADH cytosolique vers la mitochondrie. La molécule de NADH ne traversera pas la membrane. Mais les électrons rejoindront la chaine de transport. Il existe 2 navettes : La navette GLYCEROL-Phosphate La navette MALATE / ASPARTATA
3
Biochimie
a. La navette glycerol-phosphate Elle met en jeu deux enzymes : Une glycérol-3-Phosphate déshydrogénase (G3PDH cytosolique) Une flavoprotéine déshydrogénase qui contient le FAD Cette navette va permettre l’entrée du pouvoir réducteur dans la mitochondrie. Mécanisme : Les électrons sont d’abord transférés au DHAP (intermédiaire de la glycolyse). Il y a alors formation de glycérol-3-phosphate. Ce produit sera reconverti en DHAP par la flavoprotéine déshydrogénas. Cf. page 2 poly 1 Cette enzyme va transférer le pouvoir réducteur au FAD pour former FADH2. Dernière étape : transfert du pouvoir réducteur au CoQ mobile. Il le transmettra à la chaine de transport des électrons au niveau du complexe 2 ! Conséquence : synthèse de 2 moles d’ATP lors de la réoxydation du NADH de la glycolyse.
b. La navette malate / aspartate C’est un système plus complexe qui implique 2 enzymes (ASAT et MDH) et 2 transporteurs. ASAT = aspartat aminotransférase (M = 88 000) MDH = malate déshydrogénase (M = 62 000) Elles sont présentes des deux côtés de la membrane interne. But de la navette : transférer les électrons du NADH cytosolique vers le NADH mitochondrial. Les électrons vont passer du NADH sur l’oxaloacétate (l’OA). L’OA se transforme ensuite en malate. NADH + OA Malate + NAD+ (réaction rédox) La malate entrant doit traverser la membrane interne. Il utilisera un transporteur qui va l’échanger contre de l’α-cétoglutarate (α-CG C5) qui provient de la matrice. L’α-CG sorti dans le cytosol va être pris en charge par la deuxième enzyme (ASAT), ce qui va régénérer de l’OA. 4
Biochimie
Réaction ASAT : α-CG + Aspartate OA + Glutamate NB : GLU produit va traverser la membrane à l’aide du deuxième transporteur (GLU vs ASP). Celui-ci va l’échanger contre l’ASP.
Bilan : L’oxydation d’une mole de NADH par cette navette donnera, via la chaine de transport, un total de 3 moles d’ATP. NB : ASAT fonctionne avec une coenzyme phosphate de pyridoxal qui transfère les groupement amines NH2.
5...
Similar Free PDFs

3. Biochimie, Acide Nucléique
- 10 Pages

Histoire TD 3 - Notes de cours 3
- 4 Pages

Chapitre 3 - Notes de cours 3
- 4 Pages

Chapitre 3 - Notes de cours 3
- 4 Pages
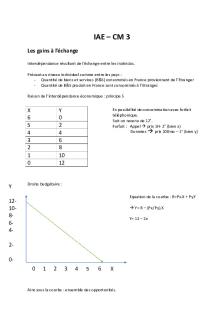
IAE – CM 3 - Notes de cours 3
- 4 Pages

Notes de cours module 3
- 7 Pages

1107 - Notes de cours 3
- 3 Pages

208 - Notes de cours 3
- 3 Pages

GEO3 - Notes de cours 3
- 2 Pages

608 - Notes de cours 3
- 3 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu





