enzimas salivales PDF

| Title | enzimas salivales |
|---|---|
| Author | aria lamda |
| Course | Bioquimica |
| Institution | Universidad de Carabobo |
| Pages | 3 |
| File Size | 183.1 KB |
| File Type | |
| Total Downloads | 102 |
| Total Views | 128 |
Summary
Download enzimas salivales PDF
Description
TAREA 5 1.- REALIZA UN DIBUJO DE LAS ENZIMAS SALIVALES (AMILASA, LIPASA, LISOZIMA) Y DESCRIBE SU ESTRUCTURA Y COMPOSICIÓN. AMILASA: Consiste en una sola cadena polipeptidica de 496 aminoacidos que se puede dividir en tres dominios. Alberga el sitio activo y contiene tres residuos catalíticos: asp197, glu233 y asp300. Las estructuras de neón son azúcares GLC utilizados con fines de cristalización. Los ligandos hidrófobos arg 377, arg 195 y asn298 funcionan como sitios de unión para iones de cloruro. La amilasa, es un enzima hidrolasa (reacción acido-base entre una sustancia, muchas veces sal y agua).
LIPASA: se caracterizan por una topología compuesta por hélices α y láminas β-plegadas. El sitio catalítico de estas enzimas generalmente está compuesto por una tríada de aminoácidos: serina, ácido aspártico o glutámico e histidina. Las lipasas son éster hidrolasas carboxílicas que rompen los enlaces éster del los acilglicéridos mediante la adición de una molécula de agua, dando lugar a ácidos grasos libres y glicerol.
LISOZIMA: Es una pequeña proteína de 130 residuos aminoacídicos y está codificada por un gen ubicado en el cromosoma 12, que posee 4 exones y 3 intrones. Esta consta de una sola cadena de 129 aminoácidos, que ha sido cocristalizada con un trisacárido que ocupa parcialmente el centro activo de la enzima: En el sitio catalítico encontramos dos aminoácidos dicarboxílicos, Glu 35 y Asp 42, que son fundamentales en la acción catalítica, La enzima presenta cuatro puentes disulfuro que mantienen su estructura terciaria.
2.- CLASIFICA LAS ENZIMAS, CITANDO EJEMPLOS DE CADA UNA Y SU ACTIVIDAD ENZIMATICA.
OXIDORREDUCTASAS: Catalizan reacciones de oxidorreducción, es decir, transferencia de hidrógeno (H) o electrones (e-) de un sustrato a otro, según la reacción general: AH2 + B A + BH2 Ejemplo, las deshidrogenasas que sustraen átomos de hidrogeno de los sustratos y los transfieren a una molécula aceptora que no es el oxígeno.
TRANSFERASAS: Catalizan la transferencia de un grupo químico (distinto del hidrógeno) de un sustrato a otro, según la reacción: ACOOH + B A + BCOOH Ejemplo, es la glucoquinasa, que cataliza la reacción representada en la Figura de la derecha:
HIDROLASAS: Catalizan la ruptura de enlaces por la adición de una molécula de agua (reacciones de hidrólisis). Según la reacción: AB + H2O AOH + BH Ejemplo, es la lactasa, que cataliza la reacción: Lactosa + agua glucosa + galactosa LIASAS: catalizan ruptura de enlaces (C-C, C-S Y C-N). Según la reacción: AB A + B Ejemplo, es la acetacetato descarboxilasa, que cataliza la reacción: Ácido acetacético CO2 + acetona ISOMERASAS: Catalizan cambios geométricos o estructurales dentro de la misma molécula (isómeros). Según la reacción: Glucosa-6-P Fructosa-6-P Ejemplo, glucosa-6-fosfato fructosa-6-fosfato
LIGASAS: Permiten la unión de dos moléculas simultáneamente a la degradación de ATP u otro enlace químico. Según la reacción: Piruvato + CO2 oxalacetato...
Similar Free PDFs

enzimas salivales
- 3 Pages

Enzimas
- 8 Pages

Glándulas salivales
- 4 Pages

Glandulas salivales
- 9 Pages

Enzimas
- 12 Pages

Enzimas
- 1 Pages

Glándulas Salivales - Anatomía
- 6 Pages

Enzimas: catalizador
- 145 Pages

Glándulas salivales mayores
- 13 Pages

Monografia de glandulas salivales
- 17 Pages
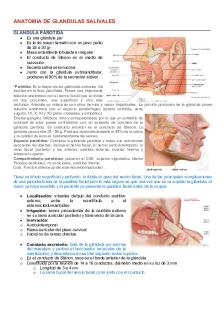
Anatomia DE Glandulas Salivales
- 3 Pages

Boca y glandulas salivales
- 2 Pages

Enzimas Plasmáticas
- 8 Pages

5. Enzimas
- 3 Pages

Estudo - enzimas
- 2 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu
