Informe 2 -Identificacion de Carbohidratos PDF

| Title | Informe 2 -Identificacion de Carbohidratos |
|---|---|
| Course | BIOQUIMICA |
| Institution | Universidad Central del Ecuador |
| Pages | 10 |
| File Size | 463.7 KB |
| File Type | |
| Total Downloads | 287 |
| Total Views | 638 |
Summary
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR CARRERA DE LABORATORIO CLÍNICO FACULTAD DE MEDICINANOMBRE Y APELLIDOSASIGNATURA FECHA DE ELABORACION DE PRACTICANOTADayana Guzmán Pablo Rayo BioquímicaJueves 12 de septiembre del 2019 FECHA DE ENTREGA DE INFORME Jueves 19 de septiembre del 2019 HORA 14 – 1...
Description
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR CARRERA DE LABORATORIO CLÍNICO FACULTAD DE MEDICINA
NOMBRE Y APELLIDOS
ASIGNATURA
Dayana Guzmán Pablo Rayo
Bioquímica
NOMBRE DE LA PRACTICA N° DE PRACTICA
FECHA DE ELABORACION DE PRACTICA Jueves 12 de septiembre del 2019 FECHA DE ENTREGA DE INFORME Jueves 19 de septiembre del 2019 HORA 14 – 16 pm
NOTA
pH y soluciones buffer 2
Objetivos: Objetivo General:
Reconocer mediante reacciones químicas los diferentes tipos de carbohidratos
Objetivos Específicos:
Identificar las pruebas para reconocimiento de carbohidratos.
Observar los cambios que producen las reacciones para la identificación de carbohidratos
Resumen: La presente práctica tiene como finalidad reconocer los diferentes tipos de carbohidratos mediante procesos químicos específicos, esto se puede observar con comportamientos físicos, es decir que cambian de color o se precipitan, pero que es una causa de una reacción química; cada carbohidrato posee cualidades específicas, ya sea por la cantidad de carbonos, enlaces o ramificaciones, los cuales reaccionaran ante compuestos determinados. Esta técnica es de gran utilidad para el estudiante ya que conoce métodos de determinación de carbohidratos que ayudaran a saber si existe azucares en liquidos o fluidos, como en orina. Es así que la metodología utilizada es añadir cada reactivo descrito en todas las soluciones y poder observar su reacción, es decir si es positivo o negativo para un compuesto en específico. Después de realizar el procedimiento necesario se obtiene resultados en cada método utilizado, fue positivo en todas las reacciones que están destinadas a
comprobar, por ejemplo en la prueba de Molish se observó un anillo rojizo purpura, determinando la presencia de carbohidratos en un compuesto. Introducción - Marco Teórico: Los carbohidratos Según McKee(2003), los carbohidratos son los compuestos orgánicos más abundantes de la biosfera y a su vez los más diversos. Normalmente se los encuentra en las partes estructurales de los vegetales y también en los tejidos animales, como glucosa o glucógeno. Estos sirven como fuente de energía para todas las actividades celulares vitales. Clasificación de los Carbohidratos Se los puede identificar y dividir siguiendo la complejidad de su estructura: 1.- Monosacáridos: Son alcoholes con 3 hasta 7 átomos de carbono que contienen un grupo aldehído o cetónico, por lo que pueden considerarse como productos de oxidación de alcoholes polivalentes en los que una función alcohólica primaria o secundaria se transforma en un grupo carbonilo (CO). Si este grupo carbonilo es terminal en la cadena, el monosacárido es una aldosa, si no se encuentra en posición terminal, el monosacárido es una cetosa. Si se toma en cuenta el número de átomos de carbono se dividen en: Triosas – Tetrosas – Pentosas – Hexosa – Heptosas Los monosacáridos más sencillos son los de 3 átomos de carbono Los monosacáridos más importantes son: Gliceraldehído y la dihidroxiacetona: ambos compuestos se encuentran en células vegetales y animales, desempeñan un papel muy importante en el metabolismo de los carbohidratos. La ribosa y la desoxirribosa: Se encuentran en la naturaleza en la forma cíclica de estructura furanosa, se encuentran en los ácidos nucleicos de todas las células vivas. La ribosa es una intermediaria en la ruta metabólica de los carbohidratos y un componente de algunas enzimas.
La glucosa: Es el azúcar más abundante en la naturaleza. Se encuentra en frutas maduras, se conoce como dextrosa. La glucosa es el azúcar circulante de los animales; la sangre contiene aproximadamente 0.08 % de glucosa. 2.- Disacáridos: Son glúcidos formados por dos moléculas de monosacáridos unidas entre sí por el denominado enlace glucosídico. Por esta razón al hidrolizarse se producen dos unidades monosacáridos. Tienen sabor dulce, cristalizan bien y son solubles en agua. El término glucosídico se refiere al enlace carbono-oxígeno-carbono que une a los dos componentes del acetal. Uno de los disacáridos más importantes es: Sacarosa: También llamada azúcar de caña o de remolacha, no se presenta en el organismo animal, aunque es un importante alimento básico, se emplea como edulcorante de alimentos. La sacarosa está compuesta de dos unidades monosacáridas diferentes, una molécula de glucosa y una molécula de fructosa, con eliminación de una molécula de agua. El cuerpo humano es incapaz de utilizar la sacarosa o cualquier otro disacárido en forma directa, es por esta razón que este disacárido se debe de fragmentarse por hidrolisis. 3) Polisacáridos: Son los carbohidratos más abundantes que existen en la naturaleza. Sirven como sustancias alimenticias de reserva y como componentes estructurales de las células. Los tres polisacáridos más importantes son: almidón, glucógeno y celulosa. Se puede hablar del almidón ya que es uno de los más abundantes en nuestro entorno. Almidón: Es el carbohidrato de reserva más importante y la fuente principal de calorías en la dieta humana. Es un polisacárido de origen vegetal que constituye la principal reserva de energía de las plantas. El almidón es un polvo blanco constituido por gránulos de estructura casi cristalina. Es insípido. Es
soluble en agua fría y al calentarse en agua tiende a formar una suspención coloidal llamada engrudo. El almidón está formado por dos fracciones estructurales: la amilosa y la amilopectina. Un método de identificación de carbohidratos y uno de los más utilizados y efectivos es la Reacción de Molisch. Reaccion de Molisch Permite detectar la presencia de hidratos de carbono en una muestra; se basa en la acción hidrolizante y deshidratante que ejerce el ácido sulfúrico sobre estos compuestos. Como se sabe, los ácidos concentrados originan una deshidratación de los azúcares para rendir furfurales, que son derivados aldehídicos del furano. Los furfurales se condensan con los fenoles para dar productos coloreados característicos, empleados frecuentemente en el análisis colorimétrico Las pentosas y hexosas ya sea tanto aldosas como cetosas; en presencia de ácidos minerales como el ácido sulfúrico y a temperaturas elevadas sufren procesos de deshidratación originando furfural (derivados de pentosas) o hidroximetilfurfural (derivados de hexosas). Los monosacáridos en caliente y medio muy ácido, sufren una deshidratación que conduce a la formación de un anillo pentagonal de furfural o hidroximetilfurfural, según se parta de pentosas o hexosas. Los oligosacáridos y polisacáridos también sufren estas reacciones, ya que el medio ácido favorece la hidrólisis previa del enlace glicosídico. Los furfurales formados se combinan fácilmente con diversos fenoles y aminas, dando reacciones coloreadas. Estos compuestos, furfural o hidroximetilfurfural, reaccionan con compuestos aromáticos (fenoles, aminas cíclicas o heterociclos) dando productos coloreados. Aunque son
pruebas
específicas
de
monosacáridos,
los
oligosacáridos y polisacáridos también dan positivo, ya que en medio ácido se hidroliza el enlace glicosídico. Se disponen de diferentes técnicas, dependiendo del reactivo utilizado. Existen otras más aparte este descrita como Prueba de Benedict, prueba de Barfoed, prueba de Seliwanoff, prueba de Bial o hidrólisis de un polisacárido
Procedimiento
Prueba de Molish
Prueba de Benedict
Prueba de Barfoed
Marcar 8 tuvos y diferenciarlos. Agregar 1mL de arabinosa, glucosa, fluctosa, galactosa, maltosa, lactosa, sacarosa y almidón; una por tubo. Añadir 2 gotas de reactivo de molish y mezclar. Colocar 10 gotas de H 2SO 4 en cada tuvo, procurando que caigan por sus paredes.
Colocar 1mL de arabinosa, glucosa, fluctosa, galactosa, maltosa, lactosa, sacarosa y almidón, en distintos tubos que permitan su identificación. agregar 5mL del reactivo de Benedict y mezclar. Someter a todos los tubos a baño maría por 5 minutos. Enfriar y observar resultados.
Agragar en distintos tubos 1mL de arabinosa, glucosa, fluctosa, galactosa, maltosa, lactosa, sacarosa y almidón e identificar. Añadir 2mL del reactivo de Barfoed y mezclar. Colocar todos los tubos en aguer hirviendo y registrar el tiempo que se tarda la presencia del presipitado rojo.
Prueba de Seliwanof
Prueba de Bial
Colocar 1mL de arabinosa, glucosa, fluctosa, galactosa, maltosa, lactosa, sacarosa y almidón, en distintos tubos que permitan su identificación. añadir 2mL de reactibo de Seliwanof y mezclar. Colocar a baño maria por unos segundos y observar resultados.
Marcar 8 tubos diferentes y colocar 1mL de arabinosa, glucosa, fluctosa, galactosa, maltosa, lactosa, sacarosa y almidón. Agregar 2 mL del reactivo de Bial y mezclar. Colocar a baño maria a todos los tuvos por par de minutos. retirar tubos y dejarlos enfriar. Se observara una tonalidad verdosa en alguno de ellos.
Hidrolisis de polisacaridos
Resultados:
Diferenciar dos tubos de ensayo y en cada uno añadir 1mL de almidon en solución. Colocar 5mL de H2SO4 solamante al primero de los tubos y mezclar. Someter a los tubos a baño maria por aproximadamente 30 minutos. retirar los tubos y dejar enfriar. añadir nuevamnete al primer tubo 5mL de H 2SO4 y mezclar. Colocar en los dos tubos reactivo de Benedict, mezclar. Observar si hay cambio en alguno.
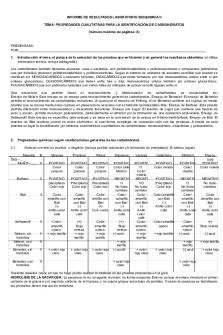
Molish Benedict Glucosa POSITIVO POSITIVO Fructosa POSITIVO Arabinosa POSITIVO POSITIVO Maltosa POSITIVO POSITIVO Sacarosa POSITIVO Lactosa POSITIVO POSITIVO Almidón POSITIVO Galactosa POSITIVO POSITIVO Tabla 1: Pruebas realizadas a carbohidratos Elaborado por: Dayana Guzmán
CARBOHIDRATO
Barfoed POSITIVO POSITIVO POSITIVO
Seliwanoff POSITIVO POSITIVO -
Bial POSITIVO -
CARACTERSITICAS Monosacárido
GLUCOSA
Monosacárido
FRUCTOSA
Monosacárido de cinco carbonos con un grupo aldehído por lo que pertenece al grupo de las aldosas y dentro de este al de las aldopentosas.
ARABINOSA
Disacárido formado por dos glucosas unidas por un enlace glucosídico α.
MALTOSA
Disacárido formado por glucosa y fructosa
SACAROSA
Disacárido formado por la unión de una molécula de glucosa y otra de galactosa
LACTOSA
Macromolécula que está compuesta de dos polisacáridos, la amilosa y la amilopectina
ALMIDÓN
Monosacárido formado por seis átomos de carbono, que se convierte en glucosa en el hígado como aporte energético
GALACTOSA
Tabla 2: Características principales de los monosacáridos analizados Elaborado por: Dayana Guzmán
En la prueba de Molish se observó la aparición de un anillo rojo púrpura en la zona de contacto que se reportó como positiva para identificación de
carbohidratos. En la prueba de Benedict se
observó la formación de un
precipitado rojo ladrillo que se reportó como positivo. En la prueba de Barfoed se observó la formación de un precipitado rojo en el fondo de los tubos. En la prueba de Seliwanoff se observó un cambio de color rosa. En la prueba de Bial al llevar la muestras a baño maría se tornaba u color azul verdoso siendo este positivo. La última prueba realizada fue la hidrolisis de un polisacárido observándose en éste un precipitado color ladrillo. Discusión de Resultados El fin de la práctica realizada fue identificar los carbohidratos mediante pruebas químicas a las cuales fueron sometidos la glucosa, fructosa, arabinosa, maltosa, sacarosa, lactosa, almidón, galactosa. La primera prueba denominada de Molish nos sirve para identificar la presencia de carbohidratos en una muestra pues todos los antes nombrados se consideran carbohidratos por tanto todos dieron positivo. La segunda prueba denominada de Benedict nos sirve para identificar la presencia de azucares reductores es decir el poder reductor de un carbohidrato se debe a las características reductoras de un grupo carbonilo es decir el carbono anomérico del carbohidrato tiene un grupo hidroxilo libre por tanto se consideraría reductor glucosa, fructosa, arabinosa, maltosa, lactosa y galactosa se consideran azucares reductoras según (Herrera, Bolaños, & Lutz, 2003). La tercera prueba denominada de Barfoed nos sirve para diferenciar los monosacáridos siendo estos los que reaccionan con mayor rapidez de los disacáridos reductores. En los disacáridos reductores el carbono anomérico de un monosacárido reacciona con un grupo hidroxilo alcohólico de otro. Así, el segundo azúcar presenta libre su carbono anomérico, y por lo tanto seguirá teniendo propiedades reductoras, y podrá presentar el fenómeno de la mutarrotación según (Voet & Voet, 2006). Por tanto los monosacáridos que reaccionaron con mayor rapidez en la práctica realizada fueron glucosa, maltosa, galactosa y por ultimo fructosa pero con menor intensidad. La cuarta prueba denominada de Seliwanoff nos sirve para diferenciar las cotosas de las adosas, como observamos en la práctica realizad las cetosas cambian de color siendo la fructosa y la sacarosa positivas, en el caso la sacarosa da positivo
porque está formada por una aldosa y una
cetosas que es la fructosa. La quinta y última prueba denominad de Bial nos sirve para identificar las pentosas y polisacáridos de pentosas en este caso la
arabinosa dio positiva porque se considera un monosacárido de cinco carbonos con un grupo aldehído por tanto se consideraría una pentosa según (Quesada, 2007). En la última prueba realizada que fue la hidrolisis del almidón en donde se observó un precipitado color ladrillo, por tanto se deduce que existe el fraccionamiento del polímero en unidades del monosacárido como son glucosa y maltosa. Conclusiones Mediante la práctica realizada se concluye que la glucosa, fructosa, arabinosa y galactosa se consideran monosacáridos y maltosa, sacarosa, lactosa se consideran polisacáridos. Las pruebas usadas en esta práctica fueron la primera prueba denominada de Molish nos sirve para identificar la presencia de carbohidratos en una muestra. La segunda prueba denominada de Benedict nos sirve para identificar la presencia de azucares reductores .La tercera prueba denominada de Barfoed nos sirve para diferenciar los monosacáridos siendo estos los que reaccionan con mayor rapidez de los disacáridos reductores. La cuarta prueba denominada de Seliwanoff nos sirve para diferenciar las cotosas de las adosas. La quinta y última prueba denominada de Bial nos sirve para identificar las pentosas y polisacáridos de pentosas Mediante la observación se concluye que en la prueba de Molish se considera positiva cuando se observa la aparición de un anillo rojo púrpura en la zona de contacto. En la prueba de Benedict se considera positiva cundo se observa la formación de un precipitado rojo ladrillo. En la prueba de Barfoed se considera positiva cuando se observa la formación de un precipitado rojo en el fondo de los tubos. En la prueba de Seliwanoff se considera positivo cundo se observa un cambio de color a rosa. En la prueba de Bial se considera positiva cuando se la muestras a baño maría por un tempo determinado y se torna color azul verdoso.
Bibliografía
Herrera, C., Bolaños, N., & Lutz, G. (2003). Quimica de Alimentos - Manual de Laboratorio. Costa Rica: Unievrsidad de Costa Rica. Masaguer, J. (1973). Investigación de sistems químicos. Barcelona: Reverté.
Quesada, S. (2007). Manual de experimentos de laboratorio para bioquímica. Costa Rica: Universidad Estatal a Distancia San Jose. Voet, D., & Voet, J. (2006). Bioquimica. Buenos Aires: Panamericana.
SlideShare (2013). identificación de carbohidratos. Recuperado el 19 de
septiembre de 2019 de https://es.slideshare.net/sextobtres/informe-de-extraccion-eidentificacin-de-carbohidratos
MedinePlus (2019).carbohidratos. Recuperado el 19 de septiembre de 2019 de https://medlineplus.gov/spanish/ency/article/002469.htm
Depa(s.f.). Análisis e identificación de carbohidratos. Recuperado el 19 de septiembre
de
2019
http://depa.fquim.unam.mx/amyd/archivero/PresentacionPractica3B_34770.pdf
de...
Similar Free PDFs

Informe N°2- Carbohidratos
- 32 Pages

Informe DE Carbohidratos - UPAO
- 7 Pages

Carbohidratos - INFORME
- 12 Pages

Informe De Carbohidratos
- 16 Pages

Informe 6 carbohidratos, química
- 22 Pages

Informe lab carbohidratos
- 11 Pages

TEMA 2. Identificacion Personal
- 9 Pages

CARBOHIDRATOS
- 48 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu