Informe De Carbohidratos PDF

| Title | Informe De Carbohidratos |
|---|---|
| Author | Leonardo Quintero Márquez |
| Course | Bioquímica |
| Institution | Universidad de Córdoba Colombia |
| Pages | 16 |
| File Size | 548.9 KB |
| File Type | |
| Total Downloads | 528 |
| Total Views | 592 |
Summary
LABORATORIO DE BIOQUÍMICAPRÁCTICA N° 4PRUEBAS CUALITATIVAS PARA CARBOHIDRATOSINTEGRANTES:CARLOS DUVAN ESPINOSA MADRIDGUSTAVO PÉREZLEONARDO QUINTERO MÁRQUEZMARIA ALEXANDRA MONTERROSA RICARDOPRESENTADO A:LUIS CARLOS DURANGO NEGRETEUNIVERSIDAD DE CORDOBAFACULTAD DE CIENCIAS BASICASPROGRAMA DE BIOLOGIAM...
Description
LABORATORIO DE BIOQUÍMICA PRÁCTICA N° 4 PRUEBAS CUALITATIVAS PARA CARBOHIDRATOS
INTEGRANTES: CARLOS DUVAN ESPINOSA MADRID GUSTAVO PÉREZ LEONARDO QUINTERO MÁRQUEZ MARIA ALEXANDRA MONTERROSA RICARDO
PRESENTADO A: LUIS CARLOS DURANGO NEGRETE
UNIVERSIDAD DE CORDOBA FACULTAD DE CIENCIAS BASICAS PROGRAMA DE BIOLOGIA MONTERÍA-CORDOBA 2020
OBJETIVOS
Reconocer la presencia de carbohidratos en una muestra problema haciendo uso de la prueba de Molish. Diferenciar carbohidratos reductores de no reductores de acuerdo a su comportamiento frente al reactivo de Benedict. Realizar ensayos cualitativos para el reconocimiento de carbohidratos específicos
INTRODUCCIÓN Los carbohidratos, hidratos de carbono o sacáridos son moléculas orgánicas compuestas por carbono, hidrógeno y oxígeno. Son solubles en agua y se clasifican de acuerdo a la cantidad de carbonos o por el grupo funcional que tienen adherido. Son la forma biológica primaria de almacenamiento y consumo de energía. Otras biomoleculas son las grasas y, en menor medida, las proteínas. Los monosacáridos, son los carbohidratos más simples y están formados por una sola molécula; no pueden ser hidrolizados a glúcidos más pequeños. Los monosacáridos poseen siempre un grupo carbonilo en uno de sus átomos de carbono y grupos hidroxilo en el resto, por lo que pueden considerarse polialcoholes. Los monosacáridos poseen siempre un grupo carbonilo en uno de sus átomos de carbono y grupos hidroxilo en el resto, por lo que pueden considerarse polialcoholes. Los oligosacáridos están compuestos por entre tres y nueve moléculas de monosacáridos que al hidrolizarse se liberan. Los carbohidratos complejos están hechos de moléculas de azúcar que se extienden juntas en complejas cadenas largas. Tanto los carbohidratos complejos como los carbohidratos simples se convierten en glucosa en el cuerpo y son usados como energía. La glucosa es usada en las células del cuerpo y del cerebro y la que no se
utiliza se almacena en el hígado y los músculos como glucógeno para un uso posterior. Glucosa: Pertenece al grupo los carbohidratos denominados simples o monosacáridos. Su molécula posee 6 átomos de carbono (hexosas), por lo que pertenece al subgrupo de las aldohexosas que son de alto interés biológico. Fructuosa: Al igual que la glucosa, la fructosa pertenece al grupo los carbohidratos denominados simples o monosacáridos. Su molécula es una hexosa y su fórmula empírica es C6H12O6. Pertenece al subgrupo de las cetohexosas que son de alto interés biológico. Galactosa: Es convertida en glucosa en el hígado y es sintetizada en las glándulas mamarias para producir la lactosa materna, conjuntamente con la glucosa. Sacarosa: Estos azúcares pueden ser metabolizados con la adición de moléculas de agua. La unión molecular de este disacárido se rompe mediante la acción de una enzima llamada sacarosa, liberándose la glucosa y la fructosa para su asimilación directa. Maltosa: Estos azúcares pueden ser metabolizados con la adición de moléculas de agua. Es fácilmente separable en moléculas simples de glucosa para su rápida utilización por el cuerpo. La
maltosa puede ser obtenida a partir de los almidones. Lactosa: Estos azúcares pueden ser metabolizados con la adición de moléculas de agua. Para separar la lactosa de la leche y ser asimilada se necesita la acción de una enzima llamada lactasa, que separa la lactosa en el intestino grueso en sus componentes más simples: la fructosa y la galactosa. Glucógeno: Es un polisacárido propio de reserva de los animales, como el almidón es el polisacárido de reserva propio de los vegetales.
MARCO TEÓRICO Las pruebas relacionadas con identificación de carbohidratos son:
la
* Prueba de Molish: Permite detectar la presencia de hidratos de carbono en una muestra; se basa en la acción hidrolizante y deshidratante que ejerce el ácido sulfúrico sobre estos compuestos. Como se sabe, los ácidos concentrados originan una deshidratación de los azúcares para rendir furfurales, que son derivados aldehídicos del furano. Los furfurales se condensan con los fenoles para dar productos coloreados característicos, empleados frecuentemente en el análisis colorimétrico. Las pentosas y hexosas (tanto aldosas como cetosas) en presencia de ácidos minerales como el ácido sulfúrico y a temperaturas elevadas sufren procesos de deshidratación originando furfural (derivados de pentosas) o hidroximetilfurfural (derivados de hexosas). Los monosacáridos en caliente y medio muy ácido, sufren una deshidratación que conduce a la formación de un anillo pentagonal de furfural o hidroximetilfurfural, según se parta de
pentosas o hexosas. Los oligosacáridos y polisacáridos también sufren estas reacciones, ya que el medio ácido favorece la hidrólisis previa del enlace glucosídico. Los furfurales formados se combinan fácilmente con diversos fenoles y aminas, dando reacciones coloreadas. *Prueba de Benedict: Es otra de las reacciones de oxidación, que como conocemos, nos ayuda al reconocimiento de azúcares reductores, es decir, aquellos compuestos que presentan su OH anomérico libre, como por ejemplo la glucosa, lactosa o maltosa o celobiosa, en la reacción de Benedict, se puede reducir el Cu2+ que presenta un color azul, en un medio alcalino, el ión cúprico (otorgado por el sulfato cúprico) es capaz de reducirse por efecto del grupo aldehído del azúcar (CHO) a su forma de Cu+. Este nuevo ion se observa como un precipitado rojo ladrillo correspondiente al óxido cuproso (Cu2O), que precipita de la solución alcalina con un color rojonaranja, a este precipitado se lo considera como la evidencia de que existe un azúcar reductor. (Aguiar T., C, etal 2014). *Prueba de Barfoed: Sirve para distinguir monosacáridos reductores de disacáridos reductores, basándose en la velocidad de reacción; en los monosacáridos la formación del óxido cuproso es más rápido que en los disacáridos. La reacción consiste en utilizar acetato cúprico y ácido acético en solución ácida con lo que los monosacáridos son capaces de reducir al cobre de manera más rápida y en condiciones menos drásticas. Por supuesto que al tener la solución un pH ácido resulta necesario controlar rigurosamente el tiempo de reacción, pues si éste se prolongara se produciría la hidrólisis ácida del enlace glucosídico con la consiguiente liberación del carbono anomérico y la
aparición de nuevos grupos reductores que falsearían el resultado. *Prueba de Bial: Cuando se calientan las pentosas en ácido clorhídrico concentrado se forma furfural que se condensa con orcinol en presencia de iones férricos para dar un color verde azuloso. En palabras técnicas, Reacción del furfural e hidroximetil-furfural con orcinol en medio con HCl, dando lugar a derivados de color azul. Es una prueba específica de pentosas.
*Prueba de Selliwanoff: Esta prueba es específica para las cetosas. Las cetosas se deshidratan más rápidamente que las aldosas, dando furfurales. Estos se condensan con el resorcinol produciendo un complejo coloreado. Si el tiempo de ebullición se prolonga, puede dar también positivo para otros azúcares. Esta prueba está basada en el hecho de que, al calentar las cetosas son deshidratadas más rápido que las aldosas. Las cetosas en el carbono 2 tienen una función cetona, que en presencia de un ácido fuerte producen rápidamente derivados furfúricos que reaccionan con un difenol llamado resorcina que está contenido en el reactivo de Seliwanoff. La sacarosa (un disacárido formado por glucosa y fructosa) y la inulina (un polisacárido de la fructosa) dan positiva la reacción, ya que el HCl del reactivo provoca en caliente la hidrólisis del compuesto liberando fructosa (responsable de la reacción positiva). *Prueba para la sacarosa: La sacarosa es el único disacárido común no reductor y por lo tanto ese reduce en las soluciones alcalinas de cobre. Además su poder no reductor se debe a que no posee carbonos anoméricos libres, por lo tanto carece de
poder reductor. Por este motivo, se debe hidrolizar la Sacarosa. Este a su vez se hidroliza en solución ácida (en presencia de HCl y en caliente), e incorpora una molécula de agua y se descompone en los monosacáridos que la forman, glucosa y fructosa, que sí son reductores resultantes. De lo resultante, después se realizan las pruebas por separado de Bennedict y Selliwanoff respectivamente.
*Prueba para polisacáridos: La reacción del Lugol (solución de yodo), es un método que se usa para identificar polisacáridos. El almidón en contacto con el reactivo de Lugol (disolución de yodo y yoduro potásico) toma un color azulvioleta característico. Esa coloración producida por el Lugol se debe a que el yodo se introduce entre las espiras de la molécula de almidón. Por lo tanto, no es una verdadera reacción química, sino que se forma un compuesto de inclusión que modifica las propiedades físicas de esta molécula, apareciendo la coloración azul violeta. (Exam, 2015).
MATERIALES Y REACTIVOS -
Estufa o calentador. Pipetas de 5 y de 10 ml. Beakers de 100 y 400 ml. 10 tubos de ensayo. Pinza para tubos de ensayo. Gradilla. Gotero. Papel Tornasol. Soluciones de glucosa, galactosa, ribosa, arabinosa, Sacarosa, lactosa, fructosa, almidón, leche*. *Traer de casa.
-
Ácido sulfúrico concentrado. Reactivo de Molish. Reactivo de Benedict. Reactivo de Barfoed. Reactivo de Bial. Alcohol Amílico. Reactivo de Selliwanoff. Ácido clorhídrico concentrado. Hidróxido de sodio 1M. Solución de yodo.
Ensayo de Seliwanoff.
Ensayo de Molisch
Ensayo de polisacáridos
Ensayo de Benedict
PROCEDIMIENTO Prueba de Molish
Se agregó 5 gotas del reactivo de Molish a 1ml de una muestra de carbohidratos (leche).
Se añadió cuidadosamente por las paredes del tubo 1 ml de ácido sulfúrico concentrado, hasta que se formen dos capas. Y se observó un cambio de color en la interfase de los dos líquidos.
Prueba de Benedict
Se tomaron 3 tubos de ensayos; al primero se agregó 0.5 ml de Lactosa, al segundo 0.5 ml de Glucosa y al tercero 0.5 ml Sacarosa.
Se adicionó 0.5 ml de reactivo de Benedict a cada tubo, con un sometimiento en baño de María por 3 minutos. Con la presencia de un precipitado de color rojo ladrillo indica la presencia de azúcar reductor.
Prueba de Barfoed
Se tomaron 3 tubos de ensayos; al primero se agregó 0.5 ml de Galactosa, al segundo 0.5 ml de Ribosa y al tercero 0.5 ml Almidón.
Se adicionó 1 ml de Reactivo de Barfoed a cada tubo, se procedió a hervir por 2 minutos y se dejó reposar. La formación de un precipitado de color rojo ladrillo indica la presencia de monosacáridos.
Prueba Bial
Se tomaron 3 tubos de ensayos; al primero se agregó 0.5 ml de Ribosa, al segundo 0.5 ml de Arabinosa y al tercero 0.5 ml Almidón.
Se adicionó 0.5 ml de Reactivo de Bial a cada tubo y se calentó hasta el punto que se empezó a hervir, se dejó enfriar, y luego se agregó 1 ml de alcohol amílico y agite, la aparición de una coloración azul verdosa es prueba positiva para pentosas.
Prueba de Salliwanoff
Se tomaron 3 tubos de ensayos; al primero se agregó 0.5 ml de Fructosa, al segundo 0.5 ml de Arabinosa y al tercero 0.5 ml Glucosa.
Se adicionó 1 ml de reactivo de Selliwanoff a cada tubo. Se calentó en baño de maría 1 minuto. La aparición de un color rojo o rosado es prueba positiva para cetosas.
Prueba para Sacarosa
A 2.5 ml de solución Sacarosa, se le agregó 3 gotas de ácido clorhídrico concentrado caliente durante 5 minutos en un baño de agua hirviendo.
Se le agregó Hidróxido de Sodio 1M hasta que la solución sea neutra o ligeramente alcalina (se prueba con el papel tornasol). Se dividió la solución hidrolizada en dos y se realizaron por separados las pruebas de Benedict y Selliwanoff.
Prueba para polisacáridos
Se Colocó 1 ml de Almidón, añada 1 gotas de solución de yodo. Se añadió 1 gotas de solución de yodo.
Además, se observó la producción de un color azul. Se calentó el tubo, y se dejó enfriar. Se procedieron a explicar las reacciones.
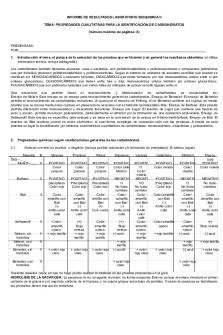
RESULTADOS P. Molish P. Benedict
P. Barfoed
P. Bial
P. Salliwanoff
P. Sacarosa
P. Polisacáridos
Leche dos fases (parte superior blanca y parte inferior morado) -Lactosa: Antes -Glucosa: Azul claro -Sacarosa: De un del calentamiento antes del calentamiento; color azul antes del azul claro; después del calentamiento; se después calentamiento Rojo sometió al sometido a baño ladrillo. calentamiento y no maría de un color hubo cambio de anaranjado. color. -Galactosa: Azul -Ribosa: Azul claro -Almidón: Azul claro antes del antes del calentamiento; claro, antes del calentamiento; a después del calentamiento; no baño maría la calentamiento un reaccionó al presencia de un precipitado rojo ladrillo. calentamiento. Por precipitado rojo tanto no hubo ladrillo. precipitado rojo de ladrillo. -Ribosa: De un color inicial amarillo, sometida a baño maría, el color presentado fue un azul oscuro. -Fructosa: De un color inicial transparente; al ser sometido al calor hubo la presencia de un color rojo.
-Arabinosa: De un color inicial amarillo; al sometimiento de calor se presentó un color azul verdoso.
-Almidón: De un color inicial amarillo; sometido al calor no reacciona, presenta el mismo color inicial amarillo.
-Arabinosa: De un color inicial transparente; al ser sometido al calor hubo la presencia de un color rojo.
-Glucosa: De un color inicial transparente; al ser sometido al calor no hubo la presencia de un color rojo. Se mantuvo su color transparente.
De una -Benedict: Al hacer la coloración blanca prueba, se presentó un amarillenta. precipitado color ladrillo.
-Salliwanoff: Al hacer la prueba, se evidenció un precipitado color rojo champagne.
De un color morazul (morado azulado). Al someterse a calentamiento, se tuvo un color verde oscuro. Después al someterse a enfriamiento, se obtuvo un color azul oscuro.
PREGUNTAS COMPLEMENTARIAS
1) Escriba cada una de las reacciones en las diferentes pruebas para carbohidratos.
REACCIÓN DE MOLISH
REACCIÓN DE BENEDICT CON LA GLUCOSA
REACCIÓN DE BARFOED
REACCIÓN DE BIAL
REACCIÓN DE SELLIWANOFF
REACCIÓN PARA SACAROSA
REACCIÓN PARA POLISACÁRIDOS
especificamente al reconocimiento de azúcares reductores. En la reacción de Benedict, se puede reducir el Cu2+ que presenta un color azul, en un medio alcalino, el ión cúprico (otorgado por el sulfato cúprico) es capaz de reducirse por efecto del grupo aldehído del azúcar (CHO) a su forma de Cu+. Este nuevo ion se observa como un precipitado rojo ladrillo correspondiente al óxido cuproso (Cu2O), que precipita de la solución alcalina de un color rojonaranja, y este precipitado se lo considera como la evidencia de que existe un azúcar reductor.
2) Explique los resultados de cada una de las pruebas realizadas.
Prueba de Molish: El ácido sulfúrico concentrado tiene la función de hidrolizar los enlaces glicosídicos para dar monosacáridos que pueden ser deshidratados dando furfural y sus derivados. Estos productos al combinarse con α-naftol sulfonato, originando un complejo púrpura. De acuerdo a esto, es la prueba general para los carbohidratos, pero algunos compuestos orgánicos dan también furfural con ácido sulfúrico concentrado. Prueba de Benedict: Es otra de las reacciones de oxidación,
Prueba de Barfoed: El reactivo de Barfoed es débilmente ácido y únicamente puede ser reducido por monosacáridos. La reacción consiste en utilizar acetato cúprico y ácido acético en solución ácida con lo que los monosacáridos son
capaces de reducir al cobre de manera más rápida y en condiciones menos drásticas. Por eso un buen manejo del pH y no dejar hidrolizar por mucho tiempo la muestra nos permite reacciones falsamente positivas, de nuevos grupos reductores.
Prueba Bial: Prueba específica para las pentosas. Cuando se calientan las pentosas en ácido clorhídrico concentrado se forma furfural que se condensa con orcinol en presencia de iones férricos para dar un color verde azuloso. En palabras técnicas, Reacción del furfural e hidroximetil-furfural con orcinol en medio con HCl, dando lugar a derivados de color azul.
Prueba Selliwanoff: Esta prueba está basada en el hecho de que, al calentar las cetosas son deshidratadas más rápido que las aldosas. Las cetosas en el carbono 2 tienen una función cetona, que en presencia de un ácido fuerte producen rápidamente derivados furfúricos que reaccionan con un difenol llamado resorcina que está contenido en el reactivo de Seliwanoff. La sacarosa (un disacárido formado por glucosa y fructosa) y la inulina (un polisacárido de la fructosa) dan positiva la reacción, ya que el HCl del reactivo provoca en caliente la
hidrólisis del compuesto liberando fructosa (responsable de la reacción positiva).
Prueba para Sacarosa: La sacarosa es el único disacárido común no reductor y por lo tanto ese reduce en las soluciones alcalinas de cobre. Además su poder no reductor se debe a que no posee carbonos anoméricos libres, por lo tanto carece de poder reductor. Por este motivo, se debe hidrolizar la Sacarosa. Este a su vez se hidroliza en solución ácida (en presencia de HCl y en caliente), e incorpora una molécula de agua y se descompone en los monosacáridos que la forman, glucosa y fructosa, que sí son reductores resultantes.
Prueba para Polisacáridos: El método que se usa para identificar polisacáridos, es la reacción del Lugol (solución de yodo), El almidón en contacto con el reactivo de Lugol (disolución de yodo y yoduro potásico) toma un color azul-violeta característico. Esa coloración producida por el Lugol se debe a que el yodo se introduce entre las espiras de la molécula de almidón. Donde se forma un compuesto de inclusión que modifica las propiedades físicas de esta molécula, apareciendo la coloración azul violeta.
2) Explique estructuralmente, por qué la maltosa es un azúcar reductor y por qué el almidón no lo es, según las observaciones.
Estructura química de la Maltosa
Maltosa: Hace referencia al azúcar de malta. Grano germinado de cebada que se utiliza en la elaboración de la cerveza. Se obtiene por hidrólisis de almidón y glucógeno. Posee dos moléculas de glucosa unidas por enlace tipo α (1-4). Sacarosa: Es el azúcar de consumo habitual, que se obtiene de la caña de azúcar y remolacha azucarera. Es el único disacárido no reductor, ya que los dos carbonos anoméricos de la glucosa y fructosa están implicados en el enlace G (1α, 2β).
4) Consulte las enfermedades producidas por el mal metabolismo de los carbohidratos
Son un grupo de enfermedades metabólicas hereditarias causadas por la ausencia del mal funcionamiento de ciertas enzimas necesarias para el funcionamiento de moléculas llamadas
Estructura química de la Sacarosa
glicosaminoglicanos qué son cadenas largas de carbohidratos de azúcar presentes en cada una de las células de nuestro cuerpo qué ayudan a construir huesos cartílagos tendones corneas la piel y el tejido conector.las personas que padecen esta enfermedad no producen suficientes cantidades de las 11 enzimas requeridas para transformar estas cadenas de azúcares proteínas y moléculas más sencillas esto produce daños celulares permanentes y progresivos que afectan el aspecto y las capacidades físicas los órganos y el funcionamiento del organismo.
La diabetes es una enfermedad en la que los niveles de glucosa (azúcar) de la sangre están muy altos. La glucosa proviene de los alimentos que consume. La insulina es una hormona que ayuda a que la gluc...
Similar Free PDFs

Informe DE Carbohidratos - UPAO
- 7 Pages

Carbohidratos - INFORME
- 12 Pages

Informe De Carbohidratos
- 16 Pages

Informe 6 carbohidratos, química
- 22 Pages

Informe lab carbohidratos
- 11 Pages

Informe N°2- Carbohidratos
- 32 Pages

CARBOHIDRATOS
- 48 Pages

Carbohidratos
- 2 Pages

Carbohidratos
- 6 Pages

Carbohidratos
- 37 Pages
Popular Institutions
- Tinajero National High School - Annex
- Politeknik Caltex Riau
- Yokohama City University
- SGT University
- University of Al-Qadisiyah
- Divine Word College of Vigan
- Techniek College Rotterdam
- Universidade de Santiago
- Universiti Teknologi MARA Cawangan Johor Kampus Pasir Gudang
- Poltekkes Kemenkes Yogyakarta
- Baguio City National High School
- Colegio san marcos
- preparatoria uno
- Centro de Bachillerato Tecnológico Industrial y de Servicios No. 107
- Dalian Maritime University
- Quang Trung Secondary School
- Colegio Tecnológico en Informática
- Corporación Regional de Educación Superior
- Grupo CEDVA
- Dar Al Uloom University
- Centro de Estudios Preuniversitarios de la Universidad Nacional de Ingeniería
- 上智大学
- Aakash International School, Nuna Majara
- San Felipe Neri Catholic School
- Kang Chiao International School - New Taipei City
- Misamis Occidental National High School
- Institución Educativa Escuela Normal Juan Ladrilleros
- Kolehiyo ng Pantukan
- Batanes State College
- Instituto Continental
- Sekolah Menengah Kejuruan Kesehatan Kaltara (Tarakan)
- Colegio de La Inmaculada Concepcion - Cebu